Målrettet cellegift kan revolusjonere kreftbehandlingen: Slik fungerer teknologien
Den raskt voksende behandlingsmetoden antistoff-legemiddelkonjugater (ADC), også kjent som målrettet cellegift, har fått stor oppmerksomhet for sin effekt i behandlingen av blant annet brystkreft. Men hvordan fungerer egentlig denne banebrytende behandlingen?
ADC-teknologien, også kjent som målrettet cellegift, har fått betydelig oppmerksomhet på grunn av sin kraftige effekt i behandlingen av flere kreftformer, inkludert blærekreft, eggstokkreft, og ikke minst brystkreft.
I en serie videoer vil HealthTalk forklare hva ADC-er er, hvordan de fungerer, og hva de kan bety for kreftomsorgen i fremtiden. Se vår første video øverst i denne artikkelen
Hva er antistoff-legemiddelkonjugater?
Antistoff-legemiddelkonjugater er en ny type kreftbehandling som kombinerer spesifisiteten til monoklonale antistoffer med den kraftige cytotoksisiteten til cellegift.
Kombinasjonen av målretting og effekt gjør det mulig å levere sterke medikamenter direkte til kreftcellene, samtidig som skaden på friske vev minimeres – et stort fremskritt sammenlignet med tradisjonell cellegift.
ADC-er består av tre hovedkomponenter som jobber sammen for å oppnå maksimal effekt: Antistoffet, cellegiften og en linker.
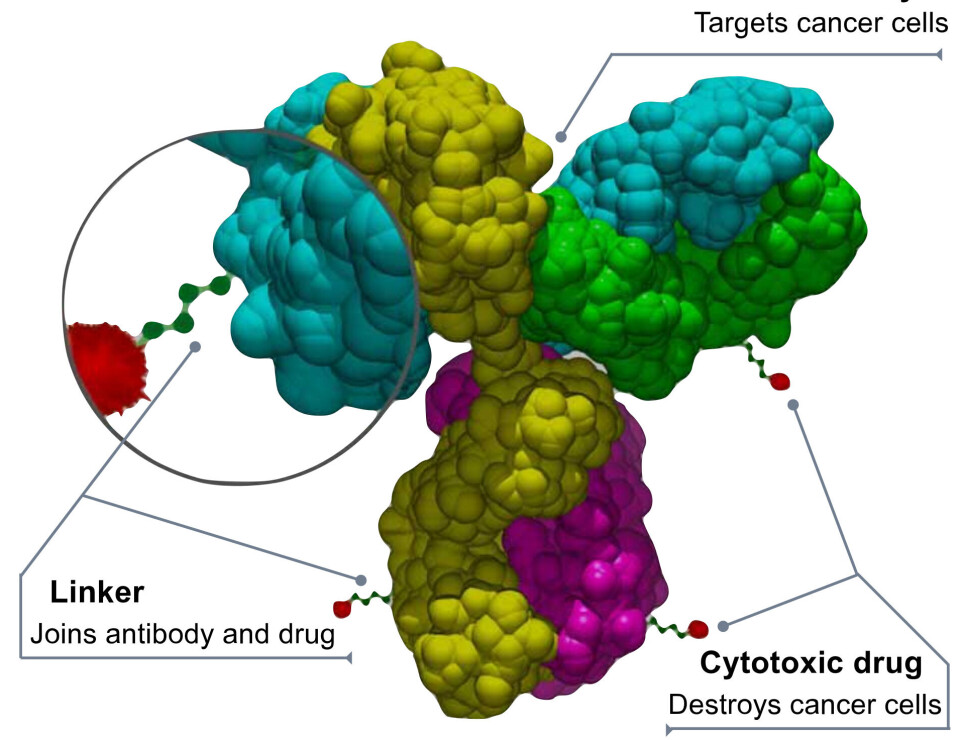
Først har vi antistoffet, som er designet for å gjenkjenne spesifikke proteiner eller antigener på overflaten av kreftcellene. Dette antistoffet binder seg til disse slik at medisinen finner sin vei til målet. Deretter har vi cellegiften, som ofte omtales som selve nyttelasten eller «stridshodet» og som slippes løs når den når kreftcellens indre.
Til slutt har vi en linker – eller bindemolekyl – som holder cellegiften festet til antistoffet inntil ADC-en har funnet kreftcellen og kan starte bekjempelsen.
Slik virker ADC-er
ADC-er fungerer ved å kreftcellene tar opp ADC-komplekset, hvor linkeren brytes ned av enzymer inne i kreftcellen. Dermed frigjøres cellegiften med sin drepende effekt på kreftcellene. Den presise leveringen av cellegift bidrar til å begrense skader på friske celler, og dermed redusere bivirkninger som hårtap og kvalme, samtidig som kreften bekjempes effektivt.
Forskerne har klart å lage linkere som er sterke nok til å bære med seg flere cellegiftmolekyler, samtidig som de hindrer ukontrollert spredning av cellegiften før de når målet. Denne presisjonen gjør at ADC-er kan målrette behandlingen mer effektivt og med færre bivirkninger enn tradisjonell cellegift.
I tillegg kan ADC-er også skape en såkalt «bystandereffekt», der cellegiften påvirker nærliggende kreftceller som kanskje ikke har det spesifikke målproteinet, men som fortsatt kan bli skadet av stoffet.
Hva har vi sett i kliniske studier?
Blant de godkjente legemidlene finner vi Genentechs Kadcyla, ImmunoGens Elahere og Gileads Trodelvy. Kreftbehandlingen har allerede gitt lovende resultater i behandlingen av flere krefttyper, og flere ADC-er er nå på vei inn i avgjørende kliniske studier.
Legemiddelselskapene undersøker også bruken av ADC-er i kombinasjon med immunterapier. Ideen oppsto rett og slett fordi det i annen behandling er vanlig å kombinere immunterapi med vanlig cellegift.
Ved å kombinere ADC-er med immunterapi håper forskere å utnytte kroppens immunforsvar for å forsterke effekten av behandlingen. Dette kan også bidra til å målrette kreftcellene enda mer presist og redusere bivirkningene ytterligere. Dermed åpnes døren for nye og mer effektive behandlingsregimer som kan kombinere ADC-teknologiens presisjon med immunterapiens muligheter.
Mye dyrere enn vanlig cellegift
Til tross for at cellegift kan være svært belastende for pasienter, er den fortsatt et kraftig våpen mot de hurtigdelende cellene som kjennetegner kreft. Dette er grunnen til at nyere behandlingsformer, som ADC-er, ennå ikke har helt klart å erstatte cellegift.
I Norge er flere ADC-er allerede godkjent. Etter hvert som enda flere ADC-er nærmer seg godkjenning, vil selskapene som har forsket frem de nye legemidlene møte flere spørsmål knyttet til økonomi og tilgang, ikke bare til effekt og sikkerhet.
ADC-er er langt dyrere enn den tradisjonelle cellegiften de kan erstatte. Dette har skapt debatt om hvor stor tilleggsverdi ADC-ene faktisk gir sammenlignet med standard cellegift, og om denne behandlingsgevinsten rettferdiggjør de høyere kostnadene.
Mens ADC-er kan gi mer målrettede og potensielt mindre toksiske behandlinger, vil deres høye pris utfordre helsevesenet når det gjelder kostnadseffektivitet og tilgang.
– Nå er spørsmålet egentlig hvor mye nytte vi trenger å se før vi godkjenner et legemiddel som sannsynligvis ikke vil være veldig billig, sa Silke Gillessen, vitenskapelig leder for ESMO og onkolog ved Oncology Institute of Southern Switzerland på ESMO i 2023.
– Det er egentlig et politisk spørsmål, konkluderte hun.



















