USA godkjenner donanemab mot tidlig Alzheimers sykdom
Amerikanske Food and Drug Administration (FDA) godkjente tirsdag donanemab, et monoklonalt antistoff designet for å bremse progresjonen av tidlig Alzheimers sykdom.
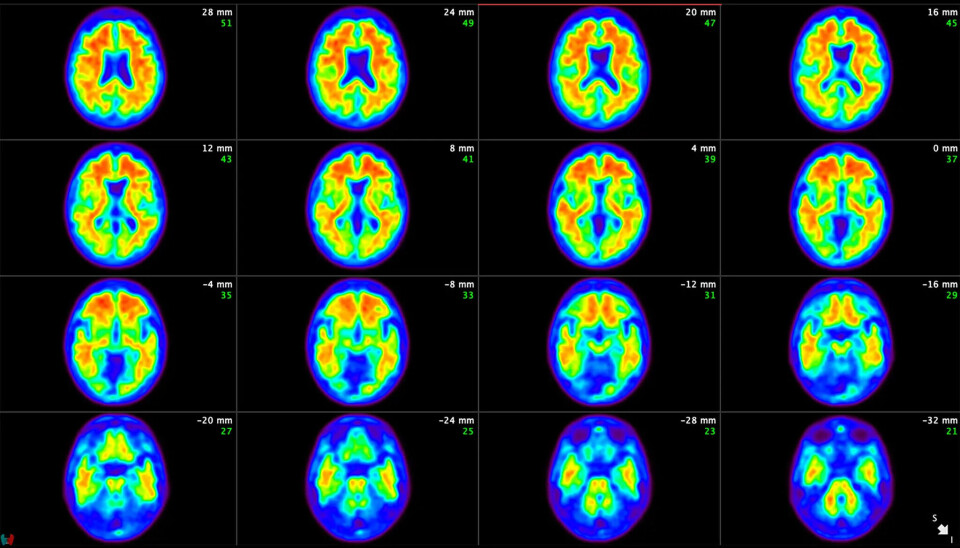
Donanemab er utviklet av Eli Lilly og virker ved å hjelpe kroppen med å fjerne amyloidplakk som bygger seg opp i hjernen, et kjennetegn ved Alzheimers sykdom. Selskapet sier i en pressemelding at medisinene fungerer best i den tidlige symptomatiske fasen av sykdommen, og at de nå jobber sammen med andre aktører for å forbedre tidlig oppdagelse og diagnose.
Kostbart
Lilly opplyser at donanemab vil bli solgt under merkenavnet Kisunla og listeprisen vil være 695 dollar per hetteglass før rabatt. Det betyr at en seks måneders behandling vil beløpe seg til 12,522 dollar og 32,000 dollar for et år, avhengig av når pasienten fullfører behandlingen.
Donanemab kurerer ikke sykdommen, men viste i kliniske studier at den bremset progresjonen av Alzheimers sykdom, slik at pasientene kunne leve selvstendige liv lenger og trygt delta i daglige aktiviteter. En senfase-studie viste at personer som tok donanemab hadde en 35 prosent lavere risiko for progresjon av sykdommen over en tidsperiode på ett og et halvt år sammenlignet med de som fikk placebo. Studien viste dessuten at risiko for at sykdommen utviklet seg til neste kliniske stadium ble redusert med opptil 39 prosent.
Ikke det første
Kisunla er ikke den første monoklonale antistoffbehandlingen som er godkjent i USA for å behandle tidlig Alzheimer. Eisai og Biogens lecanemab, solgt under merkenavnet Leqembi, er allerede i bruk. Et annet legemiddel fra Biogen, aducanumab, solgt som Aduhelm, ble i 2021 den første behandlingen som fikk akselerert godkjenning fra FDA, men selskapet har kunngjort at de vil slutte å produsere det innen utgangen av året, og vil fokusere på Leqembi.
Kisunlas indikasjon er nesten indetisk som FDA ga til Leqembi. Begge legemidlene krever bekreftelse av amyloid beta-patologi i pasientens hjernevev før behandlingen kan starte, og begge har en advarsel om risikoen for amyloid-relaterte bildeavvik (ARIA), som er kjente bivirkninger av disse antistoffene som retter seg mot de toksiske aggregatene av beta amyloid-proteiner.
Vil starte metodevurdering
Foreløpig er ingen av disse legemidlene fått markedsføringstillatelse i Europa eller Norge, men det europeiske legemiddelbyrået - EMA - vurderer i skrivende stund om lecanemab skal få markedsføringstillatelse. Aduhelm fikk avslag på markedsføringstillatelse i Europa.
Direktoratet for medisinske produkter venter nå på at Biogen og Eisai skal sende inn dokumentasjonen som er nødvendig for å utarbeide en metodevurdering av lecanemab. "Arbeidet med metodevurderingen kan begynne når fullstendig dokumentasjon er mottatt, og fageksperter er rekruttert," opplyser Direktoratet.
Konkurranse
Kisunla ble godkjent av FDA med instruksjoner om at forskrivere kan vurdere å stoppe pasientens behandling hvis de ser forbedring i amyloidplakk basert på hjerneskanninger. Ifølge Lilly kan muligheten til å avslutte behandlingen etter en begrenset behandlingsperiode bidra til å redusere behandlingskostandene. Kisunla er ellers dyrere enn Leqembi, som har en listepris på om lag 26,500 dollar per år.
En annen viktig forskjell er at donanemab vil kreve fem MR-skanninger for å sjekke for bivirkninger, mens Leqembi krever fire.
Eisai og Biogen har begynt å sende inn data til FDA som kan gi en godkjenning av en månedlig vedlikeholdsdose som skal gis som en intravenøs infusjon, samt en ukentlig injiserbar versjon av Leqembi som pasienter kan motta hjemme.
Lillys medikament forventes å bli brukt hovedsakelig av pasienter som er 65 år og eldre som er registrert i den statlige refusjonsordningen Medicare. Medicare begynte i fjor å dekke behandlingskostnadene til alzheimersmedisiner som får godkjenning fra FDA.
Leger som behandler Alzheimers, sier at godkjennelsen er et viktig steg etter flere tiår med mislykkede, eksperimentelle behandlinger.
– Jeg er svært glad for å ha forskjellige muligheter til å hjelpe pasientene mine. Det har vært vanskelig som demensspesialist – jeg diagnostiserer pasienter med Alzheimer, og så ser jeg dem bli dårligere hvert år fram til de dør, sier nevrolog Suzanne Schindler ved Washington University i St. Louis til AP.
Bivirkninger
Selv om det var sjeldent, oppstod det noen alvorlige bivirkninger hos to prosent av pasientene under de kliniske studiene. Deltakerne som tok donanemab hadde også en litt høyere dødelighetsrate: 2 prosent, sammenlignet med 1,7 % i placebogruppen.
Tre personer døde mens de tok legemidlet etter å ha utviklet ARIA (Amyloid-Related Imaging Abnormalities) som er mikroblødninger. Fordi de fleste ARIA-hendelsene skjedde i løpet av de første seks ukene av studien de la Lilly til en ekstra MR-undersøkelse i studien før de ga andre dose for å oppdage personer med asymptomatisk ARIA. Hvis det ble oppdaget, ville behandlere pause behandlingen.
















