Eli Lilly får avslag i Europa for Alzheimers-medisin – risiko vurderes som for høy
EUs legemiddelmyndigheter sier nei til Alzheimers-medisinen Kisunla fra Eli Lilly. Selv om legemiddelet er godkjent i blant annet USA, Storbritannia og Japan, vurderes risikoen for alvorlige bivirkninger som for høy til at det kan anbefales brukt i Europa.
Det var den europeiske komiteen for legemidler til mennesker (CHMP) som fredag ga en negativ anbefaling om å godkjenne Kisunla (donanemab). Årsaken er risikoen for alvorlige hjernesvulster og hevelser – såkalte amyloidrelaterte bildeavvik (ARIA) – som er påvist i behandlingsstudiene.
Ifølge CHMP veier ikke effekten på sykdomsutviklingen tungt nok opp for risikoen. Kisunla er utviklet for å fjerne plakk av proteinet amyloid beta fra hjernen – en sentral mekanisme i utviklingen av Alzheimers sykdom.
Leqembi foreløpig i tet i kappløpet
CHMPs avslag betyr at Leqembi – en konkurrerende medisin fra Biogen og Eisai – ligger an til å bli den første Alzheimers-behandlingen som godkjennes i EU. Leqembi fikk opprinnelig også et nei fra CHMP, men ble godkjent i en mer avgrenset pasientgruppe i 2023. Kun pasienter med én eller ingen kopi av APOE4-genet – som har lavere risiko for alvorlige bivirkninger – ble inkludert.
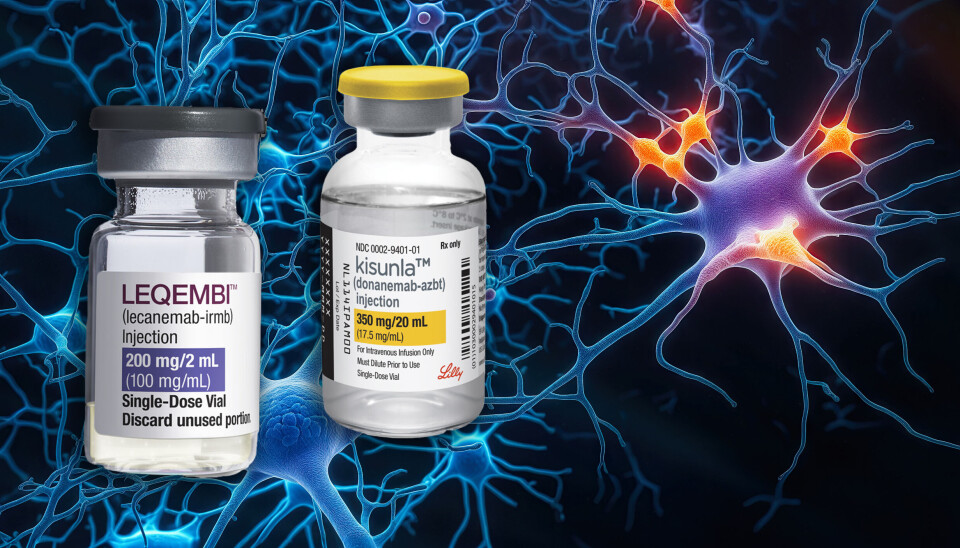
Selv om CHMP har anbefalt Leqembi i Europa, har høy pris og begrenset effekt skapt diskusjon. I USA har behandlingen en årlig kostnad på 26 500 dollar, og det er usikkert hvor bredt den vil bli tatt i bruk i kostnadsbevisste europeiske helsevesen.
– Vanskelig å forstå avslaget
Det finnes anslagsvis 7 millioner personer med Alzheimers sykdom i Europa. Reaksjonene på CHMPs nei til Kisunla har ikke latt vente på seg.
– Det er vanskelig å forstå CHMPs negative vurdering av et legemiddel som allerede er godkjent i USA, Storbritannia, Kina og Japan – og på samme vitenskapelige grunnlag, sier interesseorganisasjonen Alzheimer Europe i en uttalelse.
Eli Lilly har varslet at de vil be om en ny vurdering.