
Vil gi immunterapi fasttrack i Beslutningsforum
Helse- og omsorgsdepartementet ga i januar de regionale helseforetakene i oppdrag å følge opp evalueringen av Nye metoder, som Proba samfunnsanalyse gjennomførte på oppdrag fra departementet. Tirsdag ble rapporten overlevert helseministeren.
Dette er to av hovedgrepene som foreslås for å få ned tiden det tar å innføre legemidler:
- Legemiddelfirmaene skal selv melde legemidler inn til Systemet for nye metoder i likhet med fremgangsmåten som benyttes av Medicinrådet i Danmark. I dag skjer det basert på metodevarsler gjort av Legemiddelverket
Innføring av bestilling av metodevurderinger etter anmodning fremfor metodevarsler vil ifølge rapporten redusere arbeidsmengden for aktørene i Nye metoder og hindre bestillinger av metodevurderinger av legemidler som ikke får markedsføringstillatelse, der produsenten ikke ønsker å markedsføre sitt legemiddel i Norge, eller ikke leverer dokumentasjon.
Det innføres et forenklet godkjenningsløp for immunterapier (PD1- og PD-L1-hemmere) slik at nye legemidler og nye indikasjoner ikke trenger å gjennomgå en metodevurdering, men kan innføres så snart markedsføringstillatelse foreligger.
Sterk kritikk
Beslutningsforum for nye metoder og statsråden har fått mye kritikk for at det tar for lang til å innføre nye legemidler. 414 dager tar det i gjennomsnitt for Systemet for nye metoder å si ja til at et nytt legemiddel kan tas i bruk. I Danmark tar det 176 dager.
- Dette er for lang tid og vi jobber for å bli bedre, fortalte leder i Beslutningsforum Inger Cathrine Bryne til HealthTalk under Arendalsuka i august i år.
Legemiddelverket skal gjennomføre selve metodevurderingen innenfor en selvpålagt frist på 180 dager.
Bryne legger ikke skjul på at Systemet for nye metoder har betydelige kapasitetsutfordringer. Det gjelder særlig i Legemiddelverket som gjennomfører metodevurderinger, et av stegene legemidler må gjennom før det vurderes til offentlig finansiering. I kø står legemidler til for eksempel behandling av brystkreft, blodsykdommer, og migrene. Og listen blir stadig lengre.
I 2021 ble det bestilt 108 metodevurderinger av Legemiddelverket og som figuren under viser, klarer ikke etaten å holde tritt. Det er et stadig større sprik mellom bestilte metodevurderinger og leverte metodevurderinger. Nesten halvparten av metodevurderingene gjelder kreftlegemidler.
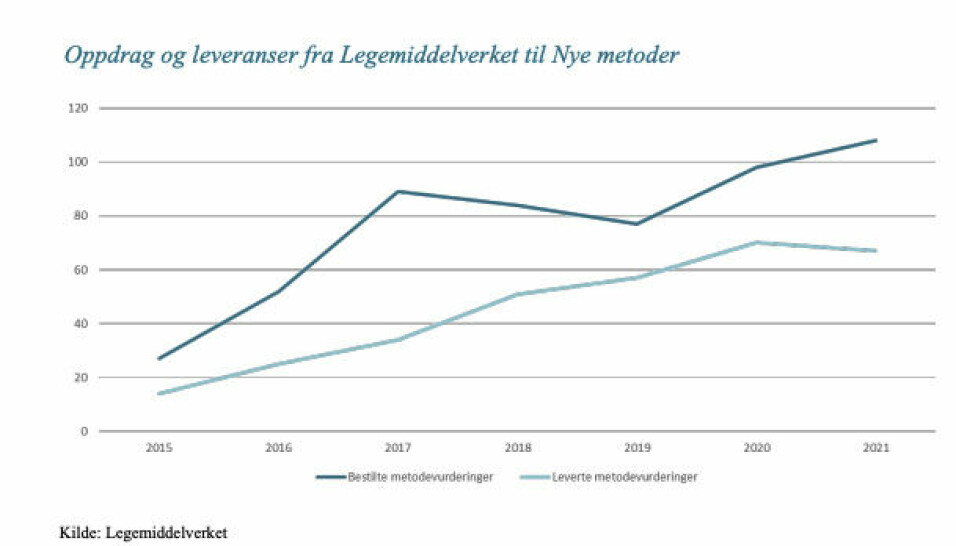
Antallet nye legemidler og nye indikasjoner har vært økende siden Nye metoder ble etablert. Det er all grunn til å anta at denne økningen vil fortsette også i de kommende år.
Pr. 07.09.2022 er det totalt 224 bestilte oppdrag for metodevurdering. Av disse er 31 metodevurderinger påbegynt mens det for 29 oppdrag er det mottatt dokumentasjon, men selve metodevurderingen er ikke påbegynt. I 164 saker venter Legemiddelverket fortsatt på dokumentasjon fra legemiddelfirma. Den økte mengden oppdrag til Legemiddelverket har bidratt til kø av saker til metodevurdering.
I rapporten understrekes det at det er uheldig at metodevurderinger ikke starter så snart den nødvendige dokumentasjonen er mottatt. Likeledes er det lite hensiktsmessig bruk av ressurser at det gjøres metodevurderinger for metoder der det er åpenbart hva utfallet av beslutningen vil bli eller der en metodevurdering ikke vil tilføre ny informasjon til saksgrunnlaget.
Rapporten slår blant annet fast at det bestilles metodevurdering i for mange saker, og at bestillingene ikke er presise på hva som er tilstrekkelig og realistisk nivå på metodevurdering.
Behov for å prioritere
Nå vil de de regionale helseforetakene tar grep for å få ned saksbehandlingstiden.
Fordi flertallet av metoder som behandles i Beslutningsforum, omkring 70 %, besluttes innført vil raskere saksbehandling bidra til at pasienter raskere får tilgang til ny behandling. Det er et overordnet mål at systemet skal bidra til raskest mulig tilgang til nye og effektive legemidler, står det i rapporten.
Her er noen av hovedanbefalingene i rapporten:
Allerede bestilte oppdrag om metodevurderinger, der Legemiddelverket har mottatt dokumentasjon, forhåndsprioriteres av Legemiddelverket basert på vurdering av alvorlighetsgrad, nytte av behandlingen og kvalitet på dokumentasjonen.
Bestilling av metodevurderinger gjøres som følge av en anmodning om vurdering fra legemiddelleverandør og ikke som i dag basert på metodevarsler gjort av Legemiddelverket. Legemiddelfirmaet som ønsker et legemiddel vurdert i Nye metoder må sende en anmodning om vurdering til sekretariatet for Nye metoder tidligst ved dag 120 (dag én for indikasjonsutvidelser og legemidler i akselerert godkjennelsesprosedyre) i godkjennelsesprosessen i EMA.
Dersom legemidler vurderes som sammenlignbart med relevant komparator, bestilles ikke ytterligere metodevurdering. Denne tidlige vurderingen, sammen med et prisnotat, vil være grunnlag for videre prosess i Nye metoder.
Det innføre en forenklet godkjenningsløp for immunterapier (PD1- og PD-L1-hemmere) slik at nye legemidler og nye indikasjoner ikke trenger å gjennomgå en metodevurdering, men kan innføres så snart markedsføringstillatelse foreligger. Dette forutsetter at det sannsynliggjøres at legemidlene har en kostnad som er under et forhåndsdefinert pristak som Beslutningsforum setter
Det er per 07.09.2022 i alt 164 bestillinger der hvor legemiddelselskapene ikke har levert dokumentasjon til Legemiddelverket. 116 av disse er fra 2021 eller tidligere. Det er derfor behov for å avslutte oppdrag der leverandørene ikke har levert dokumentasjon
– Jeg er glad for at aktørene i Nye metoder sammen har kommet frem til tiltak som blant annet kan redusere tidsbruken i systemet og styrke involvering av fageksperter og pasienter. Det er i tråd med våre forventninger. Vi har nå mottatt rapporten, og vil raskt vurdere tiltakene og behov for oppfølging, sier helse- og omsorgsminister Ingvild Kjerkol.
– I vår felles helsetjeneste vil det alltid være begrensede ressurser. Det er derfor viktig at vi har gode systemer for å treffe beslutninger som sikrer et godt og likeverdig helsetilbud over hele landet.
Forbedring innenfor rammene
- Vi jobber kontinuerlig med å videreutvikle systemet for Nye metoder. Statusrapporten som vi leverer til Helse- og omsorgsdepartementet i dag, er et solid og godt steg på veien, sier Bryne.
Framover vil Nye metoder jobbe med videreutvikling innenfor de rammene som gjelder for systemet. Samtidig er det noen faktorer som ligger utenfor selve systemet.
– Vi har et godt system for prioritering, innføring og lik tilgang av nye legemidler og metoder i Norge. Det gjøres en veldig god jobb av mange aktører allerede i dag, sier Bryne og fortsetter:
– Men vi må regne med at det også framover kan oppstå situasjoner der vi dessverre ikke kan oppnå raskere tilgjengelighet for pasientene basert på kun raskere saksbehandling. Det skjer for eksempel når leverandøren stiller et priskrav, der pris veid opp mot nytte ikke oppfyller prioriteringskriteriene vi følger, nemlig nytte, alvorlighet og ressursbruk.
































































