Legemidler og biotek
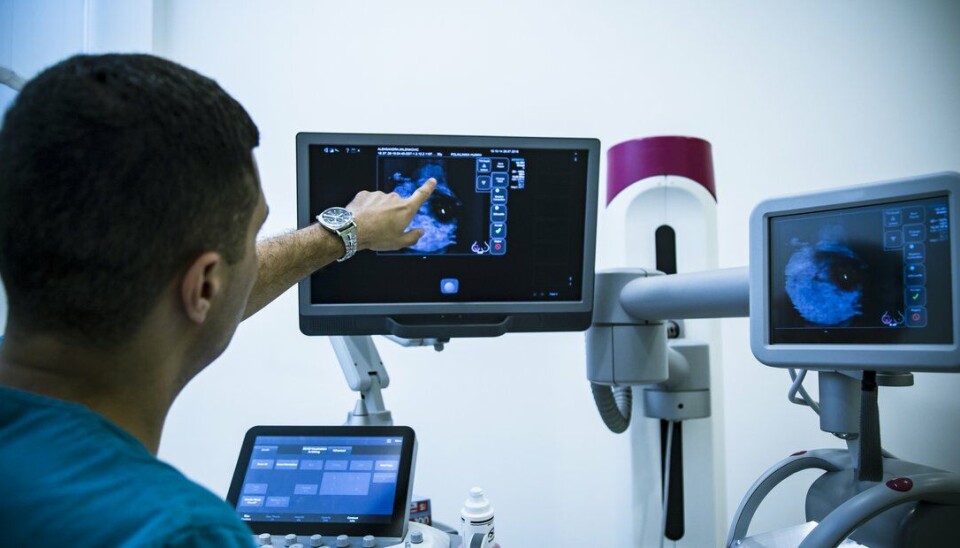
Positive resultater for Enhertu i brystkreft med lavt HER2 uttrykk
Enhertu forbedret både progresjonsfri overlevelse og totaloverlevelse i fase 3-studien DESTINY-Breast04 hos brystkreftpasienter med lavt HER2-uttrykk
Med dette har AstraZeneca og Daiichi Sankyo sitt antistofflegemiddelkonjugat (ADC) Enhertu åpnet muligheten for å bli tatt i bruk av pasienter med lavt HER2 uttrykk, som omfatter en større populasjon enn legemidlets eksisterende indikasjonsområde som er for HER2-positiv brystkreft. 55 prosent av brystkrefttilfellene regnes som HER2-lav.
I DESTINY-Breast04 viste Enhertu (trastuzumab deruxtecan) en statistisk signifikant og klinisk meningsfull forbedring i både progresjonsfri overlevelse (PFS) og totaloverlevelse (OS) hos pasienter med ikke-operabel eller metastatisk brystkreft uavhengig av hormonreseptor (HR) status. Kontrollarmen var legens eget valg av kjemoterapi.
Studien inkluderte pasienter med lavt HER2-nivå som hadde progrediert med endokrin behandling og som tidligere hadde mottatt én til to linjer med kjemoterapi i metastatisk setting.
Enhertu er nå den første HER2-rettede behandlingen som viser en overlevelsesfordel hos brystkreftpasienter med lavt HER2-uttrykk sier AstraZeneca og Daiichi Sankyo i en pressmelding.
Lavt HER2-uttrykk er klassifisert som HER2-negativ sykdom, og pasientene er derfor ikke kvalifisert for HER2-målrettede behandlinger. HER2-lav status er definert som HER2 proteinekspresjon med en immunhistokjemitest (IHC) på 1+ eller 2+, sammen med mangel på HER2-genuttrykk målt ved in-situ hybridisering (ISH) score.
Enhertu er på grunnlag av en annen studie - fase 2-studien DESTINY-Breast01 - godkjent av EMA for behandling av HER2-positiv brystkreft etter to eller flere tidligere anti-HER2-baserte regimer i metastatisk setting.
Men Beslutningsforum har imidlertid ikke innført legemidlet i Norge for denne indikasjonen, og sier de avventer nye kliniske data for andrelinjebehandling. Disse dataene er Destiny-Breast03 som viste oppsiktsvekkende resultater i en stor fase 3-studie som sammenlignet Enhertu direkte mot et annet antistofflegemiddelkonjugat - Kadcyla fra Roche- i andrelinjebehandling. Pasienter som fikk Enhertu hadde 72 prosent mindre risiko for at kreften skulle utvikle seg enn de som fikk Kadcyla. Studien ble presentert på ESMO i fjor høst og dataene er så ferske at EMA ennå ikke har godkjent Enhertu som andrelinjebehandling. Du kan lese vår omtale av denne studien her:
Enhertu er imidlertid innført i Sverige som tredjelinjebehandling.
AstraZeneca og Daiichi Sankyo sier de vil presentere detaljerte data fra DESTINY-Breast04 på en forestående medisinsk konferanse og vil dele resultatene med regulatoriske myndigheter.