Legemidler og biotek
EU godkjenner presisjonslegemidlet Padcev til behandling av blærekreft
Padcev (enfortumab vedotin) er det første legemidlet som er godkjent i EU til voksne pasienter med lokalt fremskreden eller metastatisk urotelkreft - den vanligste formen for blærekreft - som tidligere har blitt behandlet med platinabasert kjemoterapi og en immunsjekkpunkthemmer.
Godkjenningen inkluderer medlemslandene i EU samt Norge. Island og Liechtenstein og er forankret i data fra det globale fase 3-studiet EV-301 som viste en signifikant samlet overlevelsesfordel ved Padcev sammenlignet med kjemoterapi. Studien er publisert i The New England Journal of Medicine, og som nylig ble presentert ved ASCO Genitourinary Cancers Symposium 2021 (ASCO GU).
Før behandlingen kan tas i bruk i behandlingen av norske pasienter må den godkjennes av Beslutningsforum.
- Godkjenningen av enfortumab vedotin i EU er en viktig milepæl for pasienter med fremskreden urotelialt karsinom. De har i dag begrensede behandlingsmuligheter og dårlige overlevelseprognoser, sier Birgitte Claudius som er medisinsk direktør i Astellas Pharma a/s.
- Vi ser derfor frem til å samarbeide med myndighetene om å sikre disse pasientene tilgang til et nytt behandlingsalternativ så raskt som mulig.
Urotelialt karsinom er kreft som vokser ut fra epitelcellene i nyrebekkenet, urinlederne eller urinblæren. I de aller fleste tilfeller (90 prosent) er urotelialt karsinom lokalisert i urinblæren. Urotelialt karsinom i blæren er den hyppigste urologiske kreftform etter prostatakreft, samt den fjerde hyppigste kreftformen hos skandinaviske menn.
Signifikant økning i overlevelse
På global basis registreres ca. 549.000 nye blærekrefttilfeller samt 200.000 dødsfall årlig. I følge Kreftregisteret ble det i Norge i 2020 diagnostisert 1852 personer diagnostisert med blærekreft i 2020.
EV-301-studiet sammenlignet Padcev med kjemoterapi hos voksne pasienter (n=608) som hadde lokalt fremskreden eller metastatisk urotelialt karsinom og som tidligere hadde vært behandlet med platinabasert kjemoterapi og en PD-1/PD-L1 hemmer.
Padcev forbedret totaloverlevelsen signifikant, ettersom risikoen for død ble redusert med 30 prosent. På tidspunktet for den på forhånd spesifiserte interimsanalysen - etter 11,1 måneders oppfølging - levde pasientene som ble behandlet med Padcev i gjennomsnitt 3,9 måneder lenger enn pasienter som fikk kjemoterapi (12,9 måneder vs. 9 måneder, hazard ratio=0,70.). OS-fordelen med Padcev ble opprettholdt i de fleste undergruppene.
Den progresjonsfrie overlevelsen (PFS) ble også betydelig forbedret med Padcev i forhold til kjemoterapi. Gjennomsnittlig progresjonsfri overlevelse, altså tid medgått uten at kreftsykdommen progredierer, var henholdsvis 5,6 vs. 3,7 måneder for pasienter behandlet med Padcev vs. kjemoterapi. Padcev medførte dermed 38 prosents redusert risiko for sykdomsprogresjon.
Legemiddelverket skriver i et metodevarsel at median overlevelse uten kjemoterapi er samlet 3–6 måneder for pasienter med metastaser. I tidligere metodevurderinger har det blitt estimert at om lag 200-225 pasienter med lokalavansert eller metastatisk urotelialt karsinom er aktuelle for andrelinjebehandling med PD-1/PD-L1-hemmer hvert år i Norge. En del av disse pasientene vil være aktuelle for tredjelinjebehandling med enfortumab vedotin
Avansert målrettet legemiddel
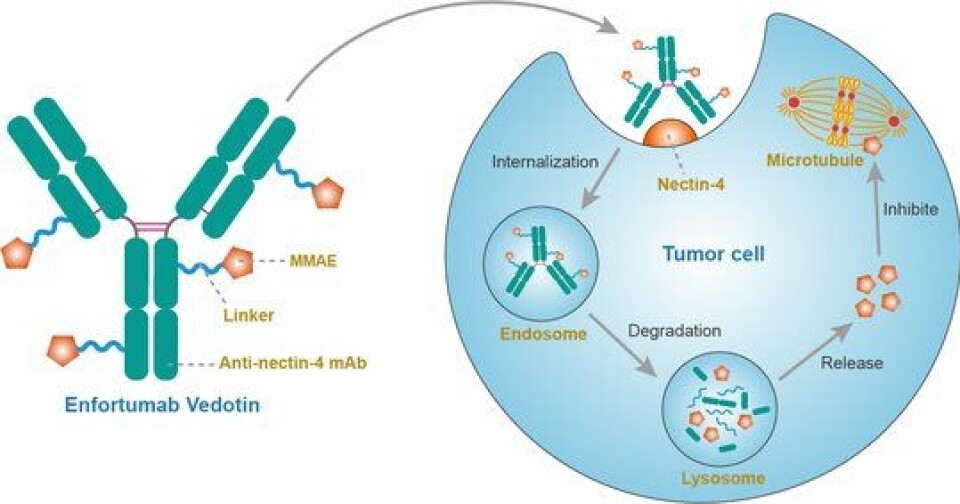
Padcev er et antistoff-legemiddel-konjugat (ADC) som tilhører en klasse kreftmedisiner som kombinerer et målrettet monoklonalt antistoff som leverer en cytotoksisk cellegift (nyttelast). Pre-kliniske data tyder på at enfortumab vedotins kreftbekjempende effekt har sammenheng med at det monoklonale antistoffet binder seg til Nectin-4, et protein på celleoverflaten som forekommer hyppig ved blærekreft, og kapsler det inn før det frigir anti-tumor-stoffet monomethyl auristatin E (MMAE) inn i cellen som så resulterer i at cellen ikke kan reprodusere seg selv (cellecyklusstopp) noe som medfører en programmert celledød (apoptose).