Legemidler og biotek, Coronaviruset
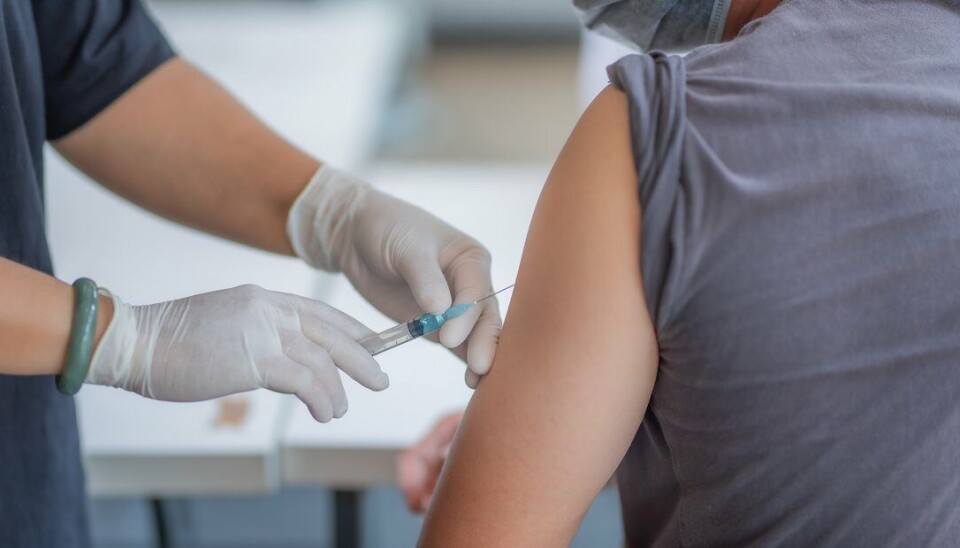
Pfizers coronavaksine BNT162b2 kan være klar i slutten av november
Dersom vaksinen viser seg å være sikker vil Pfizer søke om godkjenning av vaksinen i henhold til nødprosedyrene i den tredje uken av november. Investeringsbanken SVB Leerink tror vaksinen kan omsette for 3,5 milliarder dollar i 2021.
Det skriver sjefen for Pfizer, Albert Bourla, i et åpent brev. En nødgodkjenning - Emergency use authorization - fra det amerikanske legemiddelverket (FDA) vil innebære at helsepersonell som behandler coronapasienter og personer i risikogrupper kan få vaksinen før amerikanske myndigheter har godkjent den til allmenn bruk.
Pfizer er i tet
Pfizer ligger fremst blant legemiddelselskapene som utvikler en vaksine mot Covid-19. I brevet som ble publisert fredag, forteller Pfizer-sjef Albert Bourla i detalj når selskapet forventer å ha sikkerhets- og effektdata for den eksperimentelle coronavirusvaksinen BNT162b2 de utvikler med sin partner BioNTech, og når de vil søke den amerikanske legemiddelmyndigheten FDA om såkalt Emergency use authorization. Han forteller imidlertid ikke når Pfizer planlegger å søke EMA - den europeiske legemiddelmyndigheten - om godkjenning, men trolig vil det skje i løpet av dette året. Pfizer har en avtale med EU som kan sikre rask levering også til Norge.
Vil produsere 1, milliarder doser neste år
Bourla skriver at Pfizer trolig vil vite om vaksinen er effektiv innen utgangen av denne måneden. Det er antatt at Pfizer har besluttet at minstekravet er 50 prosent beskyttelse for at legemiddelgiganten skal velge å søke FDA om godkjenning. Men Bourla sier at Pfizer ikke vil be om Emergency use authorization før de også er sikre på at vaksinen oppfyller FDA sine sikkerhets- og produksjonskrav. De endelige sikkerhetsdataene vil være klare i midten av november. Forutsatt at vaksinen er trygg, sier Bourla at Pfizer vil sende inn en søknad til FDA i tredje uke av november.
Pfizer har investert store summer i å utvikle tilstrekkelig produksjons- og distribusjonskapasitet. Ifølge Wall Street Journal planlegger Pfizer å produsere og distribuere 100 millioner doser i år og 1,3 milliarder doser neste år.
Bøyer ikke av for politisk press
Pfizer er den eneste utvikleren av coronavaksine som vil bli i stand til å legge frem data fra en storskala studie som fastslår om vaksinen er effektiv før det amerikanske presidentvalget. Det gjør at mange frykter at godkjenningen av vaksinen kan bli politisert i den pågående amerikanske valgkampen. Det åpne brevet fra Pfizers toppsjef er et uvanlig skritt fra en legemiddelprodusent som med dette tar et aktivt grep for å overbevise opinionen om at Pfizer vil følge strenge vitenskapelige retningslinjer og ikke vil bøye seg for politisk press.
Moderna kan få godkjenning i desember
Det amerikanske bioteknologifirmaet Moderna tror at coronavaksinen de har utviklet vil få nødgodkjenning i USA i desember. Vaksinekandidaten til Moderna vil muligens bli godkjent til nødbruk dette året hvis selskapet kan vise til positive resultater fra omfattende kliniske tester i november, opplyste Modernas administrerende direktør Stephane Bancel på et arrangement i regi av Wall Street Journal mandag kveld.
Kliniske tester av to andre vaksinekandidater er blitt satt på vent i USA som følge av uventet sykdom blant deltakerne.
Først blir størst
Det er en betydelig oppside, både økonomisk og omdømmemessig, å bli det første selskapet som lanserer en coronavaksine.
Pfizer-sjef Albert Bourla har sagt nei til statlig finansiering for sin vaksinekandidat og selskapet har selv investert om lag 2 milliarder dollar i håp om å høste alle fordelene av en FDA-godkjenning. Nå som legemiddelgiganten ser ut til å ha et solid forsprang på resten, kan oppsiden bli enorm.
Investeringsbanken SVB Leerink skriver i en analyse at vaksinen - dersom den blir godkjent - trolig vil gi et salg på 3,5 milliarder dollar neste år og 1,4 milliarder dollar året etter. Bankens analytikere legger til grunn at 80% av alt helsepersonell og voksne i høyrisikosonen vil ta vaksinen, deriblant eldre og personer med kroniske sykdommer. De antar at om lag 50 prosent av voksne med lav risiko vil ta vaksinen.
Investeringsbanken skriver at de forventer at viruset blir endemisk i den menneskelige befolkningen. Vår nåværende antagelse er at vaksinerte må vaksineres hvert annet år for å opprettholde beskyttende immunitet, skriver analytikerne.
30 dollar per dose
SVB Leerink forutsetter at prisen vil være 30 dollar per dose i USA og 23 dollar utenfor USA. Banken anslår videre at den første generasjonen av vaksine kun vil være 65 prosent effektiv og at bedre vaksiner vil komme på markedet etter hvert. De forventer at vaksinen til Pfizer and BioNTech vil oppnå en markedsandel på 50 prosent, men antar også at FDA vil innvilge emergency authorizations til vaksinene til Johnson & Johnson og Moderna i løpet av året, og til Novovax, AstraZeneca og Sanofi/GlaxoSmithKline i første halvdel av neste år.































































