Kliniske studier

Regjeringen vil doble antallet kliniske studier: - Det kommer til å bli krevende.
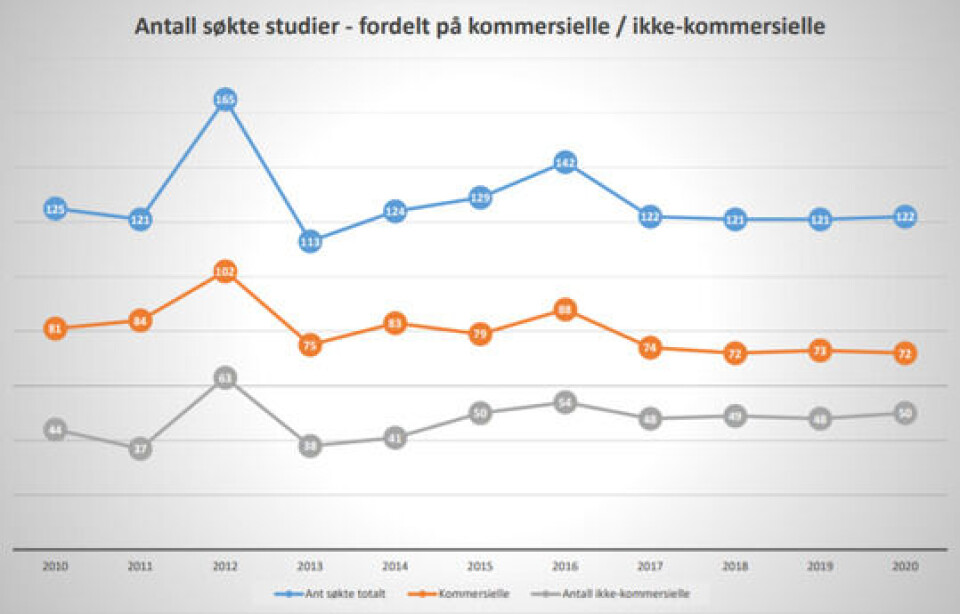
Regjeringen vil doble antall kliniske studier frem til 2025, og gjøre slike studier til en integrert del av behandlingen på norske sykehus. - Dette kommer til å bli svært krevende å få til, for i 2020 søkte industrien om å starte 72 studier mens det tilsvarende tallet året før var 73. Antallet pasienter i studiene blir dessuten færre.
Det sier Ole Kristian Hjelstuen som er administrerende direktør i Inven2. Teknologioverføringsbedriften har ansvar for å ivareta avtalemessige og økonomiske forhold i kliniske studier og industrisamarbeid som er helt eller delvis finansiert av industri. Inven2 har ansvar for kliniske studier for ni helseforetak i Helse Sør-Øst og for Universitetssykehuset Nord-Norge.
Tall fra Statens legemiddelverk viser at antallet legemiddelstudier finansiert av industrien ble mer enn halvert fra 2000 til 2010, og har med unntak av 2012 ligget på et stabilt lavt nivå siden da. Men situasjonen er verre enn det som kommer frem når man ser på antallet studier som igangsettes i Norge.
Her kan du se et intervju med Ole Kristian Hjelstuen
Færre pasienter i studiene
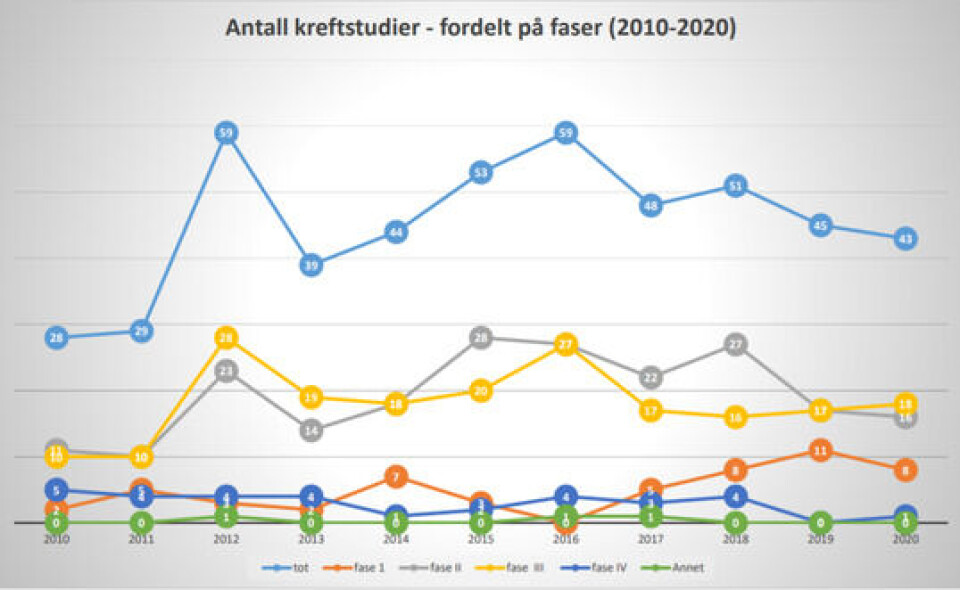
- Det er færre pasienter nå som får tilbud om å være med i kliniske studier. Det skyldes at nedgangen har vært størst i fase 3-studiene som inkluderer flere pasienter enn tidligfasestudiene. Antallet pasienter som får tilgang til utprøvende behandling gjennom kliniske studier er derfor redusert mer enn antallet studier alene skulle tilsi, forteller Hjelstuen.
Med dette bakteppet la Regjeringen i januar i år frem den aller første nasjonale handlingsplanen for kliniske studier. Ambisjonen er stor. – Regjeringens mål er å doble antall kliniske studier innen 2025. Mange flere pasienter skal delta i kliniske studier, og kliniske studier skal være en integrert del av behandlingstilbudet til pasienter. Det skal gjøre fagmiljøene bedre i stand til å ta i bruk ny kunnskap, og bidra til at flere pasienter får muligheten til å prøve ut ny, lovende behandling, sa helse- og omsorgsminister Bent Høie, da handlingsplanen ble lagt fram
- Det er lett å se hvorfor regjeringen ønsker flere kliniske studier i Norge: Kliniske studier er nøkkelen til medisinsk utvikling. Slike studier kan gi svar på hvilken behandling som er mest effektiv, sikker og kostnadseffektiv for pasienter som behandles av det norske helsevesenet. Studiene gir også norske pasienter tilgang til ny behandling flere år før den innføres i ordinær behandling. I tillegg får norske leger og sykepleiere tidlig kunnskap og verdifull erfaring med de nye legemidlene som er viktige for at det norske helsevesenet skal holde tritt med den rivende medisinske utviklingen, sier Hjelstuen.
- Regjeringen sier at de vil doble antall kliniske studier innen 2025. Er det en realistisk målsetning?
- Det er i hvert fall en god ambisjon, og vi ser at det skjer veldig mye positivt i helseforetakene som en respons på handlingsplanen. Så er jo spørsmålet om det er mulig for helseforetakene å gjøre seg tilgjengelig for så mange studier. Et annet spørsmål er om det er så mange studier som på såpass kort tid vil kunne legges til Norge. Det avhenger av flere ting enn at bare sykehusene kan og vil. Mye ligger utenfor deres kontroll, sier Hjelstuen.
Han forteller at ett problem er at flere av de globale legemiddelselskapene svekker sin tilstedeværelse i Norge. Dessuten tar det ofte lang tid å få innført nye innovative legemidler i det offentlige helsevesenet, og regjering og Stortinget har som strategi at prisene på legemidler i Norge skal være blant de laveste i Europa. - Kombinasjonen med lang tid før et legemiddel blir innført at det norske markedet er ganske lite og lav pris gjør nok at det blir mindre attraktivt for de globale legemiddelfirmaer å investere i kliniske studier i Norge sammenlignet med andre europeiske land, sier Hjelstuen.
Han forteller at til tross for pandemien har de norske studiestedene klart å levere og at det har gitt utslag i at Norge har fått flere studier den siste tiden.
- Vi har merket at handlingsplanen skaper positive ringvirkninger både i sykehusene og blant legemiddelfirmaene. Men hvis økningen kommer i 2021 eller tidlig i 2022 så skyldes det kanskje like mye at norske fagmiljøer har vært operative og dyktige i å gjennomføre kliniske studier selv under COVID-19 pandemien som effektene av handlingsplanen. Det at studiene ikke har blitt nevneverdig forsinket under pandemien har blitt lagt merke til og har medført at vi fikk tilført flere studier høsten 2020 - og vi ser at det også er tendensen så langt i 2021. Jeg tror det er mulig ri på denne bølgen og forsterke den og få til en betydelig økning frem mot 2025, sier Hjelstuen.
- Hva skal til for at vi i skal klare å få flere internasjonale studier til Norge?
- Da er det viktig at vi bygger på det som fungerer, på de styrkene vi har. Alle som bidrar må gjøre mer. Vi ser at de fagmiljøene som er gode tiltrekker seg studier, og når de tar en lederrolle som nasjonal koordinator betyr det at andre og mindre sykehus kan bli med på den samme studien. Det er derfor viktig at vi i første omgang styrker disse fagmiljøene og at de tar ansvar, slik at de kan dra med seg fagmiljøer og leger som ikke i samme grad er etablert. Det er litt som tanken bak Olympiatoppen - som har som mål å utvikle de beste utøverne til å bli best i verden i konkurranse med utøverne fra andre land – ikke i konkurranse innad i eget land.
- Danmark har lykkes i å bli en ledende europeisk forskningsnasjon, med et stort antall kliniske studier i forhold til befolkningsstørrelsen. Har de en suksessoppskrift som vi kan lære av?
- Ja, men vi må være klar over at våre to land er forskjellige. I Danmark er legemiddelindustrien og helsenæringen det som oljenæringen er for Norge. Den danske regjeringen snakker om kliniske studier når de møter sine kolleger fra andre land og ambassadene deres spiller også en aktiv rolle. Vi har en god vei å gå før vi er på nivå med den danske modellen. Vi kan og bør selvsagt lære av danskene, men det viktigste tror jeg er å styrke det som allerede fungerer i Norge. Det er tøff konkurranse om å tiltrekke seg internasjonale studier og det krever at de store universitetssykehusene går i front og får med seg de andre sykehusene, sier han.
- Hva kan dere i Inven2 gjøre?
- Vår spesialoppgave er å ivareta avtalemessige og økonomiske forhold i kliniske studier mellom industrien og helseforetakene Helse Sør-Øst og Universitetssykehuset Nord-Norge. Vi gjør det for 85 prosent av alle industristudiene. Det som vi kan bidra med er først og fremst å korte ned tiden fra avtale er signert til studien starter. Det er et konkurransefortrinn for Norge som vi utnytter aktivt, sier Hjelstuen.
Hans Anderssen, redaktør i HealthTalk
Vi i HealthTalk ønsker å lage innhold som er verdifullt for deg som jobber i helsevesenet. Hvis du likte denne artikkelen, og vil at vi skal lage mer innhold som dette, kan du støtte oss ved å melde deg på vårt nyhetsbrev her
































































