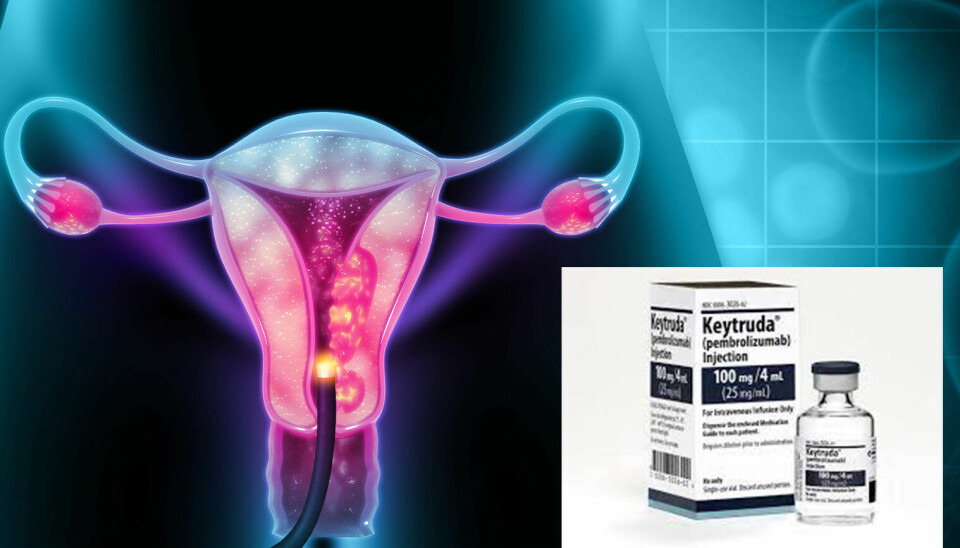
De positive dataene kan potensielt gi en FDA-godkjenning for Keytruda som en førstelinjebehandling av livmorkreft.
Foto: Getty Images
Immunterapi pluss kjemoterapi bedre enn kjemoterapi i førstelinje livmorkreft
Immunterapien Keytruda brukt sammen med standard kjemoterapi er bedre enn kjemoterapi alene til å avverge tumorprogresjon eller død (PFS) ved avansert eller tilbakevendende endometriekarsinom.
Livmorkreft eller endometriekreft er den hyppigste gynkreftformen i Norge, og faktisk den eneste som stiger i insidens. Livmorkreft utgår fra livmorslimhinnen, rammer først og fremst kvinner etter overgangsalderen og har en insidens på om lag 800 nye pasienter pr år i Norge. Livmorkreft oppstår når celler i livmoren begynner å dele seg og vokse uten hemning.
Annonse kun for helsepersonell
Beslutningsforum sa nylig nei til å innføre immunterapien Keytruda i kombinasjon med det målrettede legemidlet Lenvatinib som andrelinjebehandling av pasienter med avansert eller tilbakevendende livmorkreft. Behandlingskombinasjonen har godkjenning i Europa, men Beslutningsforum konkluderte på sitt møte i september 2022 at “behandlingskostnaden er for høy i forhold til dokumentert klinisk nytte.” Med offentlige priser på Keytruda + Lenvima koster en måned med kombinasjonsbehandlingen om lag 140 000 kroner (uten merverdiavgift) for en pasient. Dersom pasienten behandles i ett år, koster kombinasjonsbehandlingen nesten 1 million kroner.
Men nå har MSD presentert data fra en studie der de har testet ut immunterapien sammen med standard kjemoterapi som førstelinjebehandling. Keytruda, brukt sammen med standard kjemoterapi (paclitaxel and carboplatin) er bedre enn kjemoterapi alene til å avverge tumorprogresjon eller død (PFS) ved avansert eller tilbakevendende endometriekarsinom, forteller MSD. Forbedringen var statistisk signifikant og klinisk meningsfull, la selskapet til.
De positive dataene kom fra fase 3-studien NRG-GY018 som er sponset av det amerikanske National Cancer Institute.
Annonse kun for helsepersonell
MSD sier de vil diskutere resultatene med regulatoriske myndigheter. Dataene kan potensielt støtte en søknad om markedsføringstillatelse til FDA og EMA.