Legemidler og biotek
Novartis forhandler med Sykehusinnkjøp om genterapi som kan hindre at barn blir blinde - diskuterer resultatbasert prising
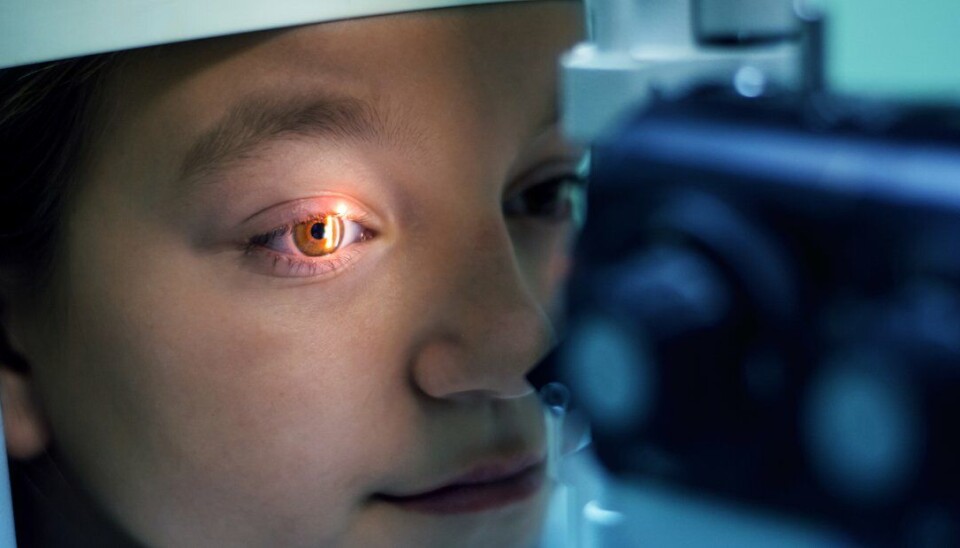
Barn med den arvelig sykdommen retinal dystrofi er født svaksynte og blir blinde i ung alder. Nå finnes det en genterapi som kan redde synet. Luxturna er innført i Danmark, men Beslutningsforum har sagt nei til at behandlingen som koster nesten 9 millioner kroner kan tilbys norske pasienter. Novartis er nå i forhandlinger med Sykehusinnkjøp. En løsning som nå diskuteres er at helseforetakene kun skal betale for behandlinger som har en varig effekt - såkalt resultatbasert prising.
Begrunnelsen for avslaget er at prisen som Novartis tilbød “var alt for høy”. Beslutningsforum var også i tvil om at effekten av engangsbehandlingen er langvarig. Novartis har gitt et nytt pristilbud og er nå i forhandlinger med Sykehusinnkjøp. Etter forhandlingene er gjennomført skal Beslutningsforum ta en ny vurdering om genterapien skal innføres.
Behandling av sykdom med genterapi er i rask utvikling. Genterapier er utviklet for å være en engangsbehandling og en kur for sykdom. Prisen er imidlertid svært høy, noe som gjør det krevende å få innpass i et beslutningssystem som er innrettet mot å gi refusjon til kronisk terapi fremfor engangsbehandling.
Novartis har to genterapibehandlinger som har fått markedsføringstillatelse i Norge - Zolgensma mot sykdommen spinal muskelatrofi og Luxturna mot retinal dystrofi også kalt Lebers medfødte synstap.
Zolgensma har ennå ikke vært opp til vedtak i Beslutningsforum. Zolgensma er kjent som verdens dyreste legemiddel og har en listepris (maksimal AUP) på om lag 20 millioner kroner før eventuell rabatt.
Den 30. mars i fjor hadde Beslutningsforum Luxturna oppe til vurdering. Men de fire direktørene for de regionale helseforetakene valgte å ikke innføre genterapien. De begrunnet vedtaket med at prisen - selv etter at Novartis hadde rabattert listeprisen - var alt for høy og at det er usikkerhet om effekten av engangsbehandlingen holder seg over tid.
Blir blinde i ung alder
Luxturna er en genterapi til behandling av synstap på grunn av arvelig retinal dystrofi som skyldes mutasjoner i RPE65-genet. Mennesker med RPE65-mutasjoner er født svaksynte og blir blinde i ung alder. Når tilstanden diagnostiseres i barndommen, vil den alltid føre til blindhet innen voksenalderen. En genetisk test er nødvendig for å bekrefte at synstapet er forårsaket av mutasjoner i RPE65-genet.
Disse mutasjonene hindrer netthinnen i å lage et protein som er nødvendig for synet. Virkestoffet i Luxturna er et modifisert virus som inneholder en normal kopi av RPE65-genet. Luxturna injiseres under netthinnen og tilfører en fungerende kopi av RPE65-genet, som erstatning for det muterte genet. Etter injeksjonen leverer viruset genet til cellene i netthinnen slik at denne normale genkopien kan brukes til å produsere det manglende proteinet. Pasienten må ha tilstrekkelig med levedyktige netthinneceller for å kunne få behandling med Luxturna.
Listeprisen er 8,9 millioner kroner
Det finnes i dag ingen tilgjengelig behandling i Norge som kan bremse synstapet ved arvelig retinal dystrofi. Dagens tilbud er optimalisering av synsrestfunksjonen gjennom ulike synshjelpemidler og hjelp til mestring av synshandicap - såkalt best supportive care - BSC.
Kliniske studier av Luxturna har vist god effekt av denne genterapien. Etter behandling kunne 62 % av pasientene navigere rundt i en labyrint ved den laveste lyssettingen (skumringslys), mot 0 % i kontrollgruppen som ikke hadde fått behandling.
I sin kostnads-nytte-analyse vurderer Legemiddelverket at merkostnaden per vunnet kvalitetsjustert leveår (QALY) for Luxturna sammenliknet med BSC er 2,4 millioner kroner.
Luxturna har en listepris på 8,9 millioner kroner for behandling av begge øynene. I følge Beslutningsforum er det i dag 8 pasienter som aktuelle for behandling med genterapien og det forutsettes at 4 pasienter per år får behandlingen. Senere er det aktuelt å behandle 1 pasient per år. Samlede budsjettkostnader før rabatt fra Novartis (maks AUP) er beregnet til 35 millioner kroner inklusive moms. I etterfølgende år vil det være en total årlig budsjettkonsekvens på i underkant av 9 millioner kroner.
Pågående forhandlinger
Den 30. mars i fjor vedtok som nevnt Beslutningsforum å ikke innføre Luxturna. Begrunnelsen var at prisen var alt for høy og at det er usikkerhet om effekten av engangsbehandlingen holder seg over tid.
Nå har Novartis kommet med et nytt pristilbud, og selskapet er i skrivende stund i forhandlinger med Sykehusinnkjøp. Det får HealthTalk bekreftet av både Sykehusinnkjøp og Novartis. Forhandlingene er krevende. Myndighetenes hovedregel om kun flat rabatt kan hindre pasienters tilgang til genterapien.
Med dagens refusjonssystem for legemidler i spesialisthelsetjenesten må Novartis redusere prisen til under halvparten av listeprisen for at Beslutningsforum skal si ja til at norske pasienter skal få behandling med genterapien. En flat rabatt på denne størrelsen sitter trolig langt inne for Novartis. Det vet selvsagt Sykehusinnkjøp som har som en del av sin strategi at “Det skal være forretningsmessig interessant for leverandører å tilby nye legemidler og løsninger”.
HealthTalk er kjent med at partene nå diskuterer flere ulike avtalemodeller som ikke bare dreier seg om hvor mye Novartis må rabattere for at Sykehus skal si seg fornøyd, og for at Beslutningsforum skal velge å innføre legemidlet.
Forhandler om en "Dansk modell"
Det som peker seg ut som en balansert avtaleløsning er å kopiere modellen som brøt isen i Luxturna-forhandlingene mellom Novartis og det danske Medicinrådet. Utfordringen er at en “Dansk modell” ikke tidligere har vært brukt i Norge. Strategien til Sykehusinnkjøp er nemlig å oppnå faste rabatter på listepris (AUP - apotekenes utsalgspris).
Resultatbasert pris og avdragsbetaling
27. april i fjor vedtok Medicinrådet å innføre Luxturna som standardbehanding i Danmark basert på en prismodell der helseregionene betaler for legemidlet i avdrag i stedet for hele beløpet på en gang - og at de kun betaler for behandlinger som har en vedvarende effekt. Pasientene skal nemlig til kontroll på fastsatte tidspunkter, og hvis det viser seg at legemidlet ikke har den ønskede effekt så skal de etterfølgende avdragene ikke betales. Dersom legemidlet virker, er prisen den samme som ved det tidligere tilbudet.
- Selvfølgelig så vi heller at Novartis hadde gitt en større rabatt, for selv med den nye betalingsmodellen er Luxturna ekstremt dyr. Men vi er glade for å kunne anbefale et lovende legemiddel, fordi vi tross alt har fått et tilbud som er bedre enn det forrige, sa Medicinrådets leder Jørgen Schøler Kristensen i april i fjor.
Første gang Luxturna var opp til behandling i Medicinrådet var i september 2019. Da uttalte Medicinrådet at legemidlet hadde en “viktig klinisk merverdi”, men valgte den gang å ikke anbefale det som standardbehandling, fordi “prisen var satt urimelig høyt og at det var usikkerhet om langtidseffekten av legemidlet og eventuelle bivirkninger.” Den gang oppfordret Medicinrådets leder Novartis å komme tilbake med et bedre og lavere pristilbud for pasientenes skyld.
Forhandlinger pågår
Hanne Eriksson er Novartis sin Cluster Commercial Lead i Gene Therapy Ophthalmology Nordics. Hun bekrefter at de har foreslått en dansk prismodell i de pågående forhandlingene med Sykehusinnkjøp. Hun vil imidlertid ikke si noe om prisen eller konkret om modellen som nå ligger på forhandlingsbordet.
Er slik resultatbasert prising (Pay for Performance) innebærer at Sykehusinnkjøp og Novartis inngår en avtale der myndighetene betaler for den faktiske helsegevinsten oppnådd med behandlingen. Hva som defineres som oppnådd helsegevinst vil avgjøres av avtalen. Forhold som respons og varighet av respons vil typisk være resultater man kommer til å vektlegge i en slik avtale.
- Vi er i disse dager i forhandlinger med Sykehusinnkjøp, og jeg kan derfor ikke kommentere detaljene forhandlingene. Det finnes et sterkt ønske blant pasienter og klinikere om at Luxturna blir tilgjengelig siden det finnes pasienter med et akutt behov og studiene som ligger til grunn for markedsføringstillatelsen viser en tydelig dokumentert effekt ved behandling av Luxturna. Samtidig ligger det i sakens natur at det finnes usikkerhet rundt langtidseffekt, som er typisk for genterapier som Luxturna. I Storbritannia valgte NICE (tilsvarende Statens legemiddelverk, red.anm.) å legge til grunn 40 års effektvarighet i den endelige refusjonsanbefalingen, på bakgrunn av at det er ansett som biologisk plausibelt at effekten er så langvarig, sier Hanne Eriksson til HealthTalk.
- Har dere fått gehør for en ny prismodell?
- Vi har en god og konstruktiv dialog med Sykehusinnkjøp der vi har lagt frem ulike forslag, blant annet innkjøpsmodeller som baserer seg på tilsvarende konsept som man har i Danmark, der myndighetene kun betaler dersom behandlingen har en vedvarende effekt, sier hun.
Sykehusinnkjøp og Nye metoder ønsker ikke å stille til intervju med HealthTalk om de pågående forhandlingene og deres vurderinger knyttet til en dansk modell. I stedet skriver kommunikasjonsleder Kjersti S. Lien i Sykehusinnkjøp dette i en mail til HealthTalk.
"Vi har mottatt et nytt pristilbud fra Novartis som er forelagt interregionalt fagdirektørmøte. Sykehusinnkjøp er bedt om å gå i ny dialog før saken fremmes for Beslutningsforum."
Ellen Nilsen er enhetsleder i sekretariatet for Nye metoder. Hun skriver dette i en e-post:
"Beslutningsforum besluttet 30.03.20 at det var ønskelig å ta Voretigene neparvovec (Luxturna) i bruk for Lebers medfødte synstap, men den tilbudte prisen var altfor høy og det var usikkerhet rundt langtidseffekten. Etter dette har det vært en forhandlingsprosess mellom Sykehusinnkjøp HF og firmaet Novartis for å komme fram til en avtale som kunne være forenlig med Stortingets vedtatte prinsipp for prioriteringer i helsetjenesten."
Er åpne for å diskutere nye innkjøpsmodeller
Novartis håper Beslutningsforum vil være villig til å teste ut nye innkjøpsmodeller.
- Rammeverket for refusjon av av legemidler tar ikke i tilstrekkelig grad hensyn til egenarten ved genterapibehandlinger. Andre helseøkonomiske organer, som NICE i England, har opprettet et separat rammeverk for å ta høyde for egenskapene som genterapi representerer. Vi håper at også norske myndigheter kan få plass et tilsvarende rammeverk. Vi oppfatter vi at norske myndigheter er åpne for å diskutere alternative innkjøpsmodeller, så vi er optimistiske til at vi skal komme til en løsning som vil gi norske pasienter tilgang til Luxturna, sier Hanne Eriksson i Novartis.
Eriksson forteller at i tillegg til Danmark, så har også Tyskland, England, Frankrike, Italia, Nederland, Østerrike, Kroatia og Israel innført genterapien .
Sverige sa nei
I Sverige er det TLV - Tandvårds och Läkemiddelsformånsverket - som utarbeider en rapport om helseøkonomien (tilsvarende en metodevurdering) til et nytt legemiddel og deretter tar NT-rådet (Rådet för Nya Terapier) en beslutning om legemidlet skal innføres eller ikke. I oktober 2019 vedtok NT-rådet å ikke innføre Luxturna.
“Prisen selskapet ber om er rett og slett for høy. Vi har hatt en diskusjon med selskapet om prisen, men dessverre har vi ikke klart å bli enige om et rimelig prisnivå. Samfunnet betaler gjerne for effektive medisiner, men når det gjelder en behandling der effekten er veldig langt inn i fremtiden, må det være betydelig sikkerhet i den antagelsen. NT-rådet kan akseptere usikkerhet om langsiktige effekter, men da må selskapet tilby en betydelig lavere pris, sa NT-rådets leder Gustaf Befrits, da avslaget ble gitt.
- Det er riktig at vi fikk en negativ beslutning av svenske myndigheter, men vi befinner oss i en pågående dialog og håper vi kan komme til enighet her på lik linje med øvrige europeiske land, sier Hanne Eriksson.
Novartis er åpen for en dansk modell eller andre løsninger som vi kan utvikle sammen med norske myndigheter. For Novartis er det viktig at Luxturna blir tilgjengelig for norske pasientene og at det eksisterer en åpenhet for å ta i bruk nye innkjøpsmodeller som kan adressere usikkerhet som typisk er knyttet til slike behandlinger, sier hun.
Hans Anderssen, redaktør i HealthTalk


Vi i HealthTalk ønsker å lage innhold som er verdifullt for deg som jobber i helsevesenet. Hvis du likte denne artikkelen, og vil at vi skal lage mer innhold som dette, kan du støtte oss ved å melde deg på vårt nyhetsbrev her
































































