Helseteknologi
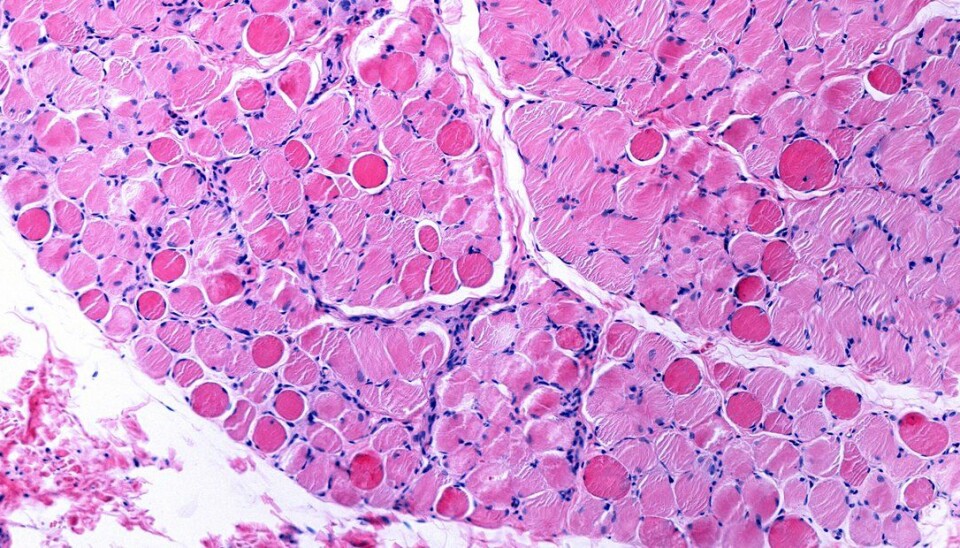
Genredigering reverserte mutasjon hos mus med Duchennes muskeldystrofi
For første gang har man ved hjelp av genredigering klart å reversere en genmutasjon, kalt duplikasjonsmutasjon, hos et levende forsøksdyr.
Korrigerte genmutasjon
Ved å gi en laboratoriemus den eksakte mutasjonen som forekommer hos pasienter med Duchennes muskeldystrofi, DMD, har man ved hjelp av genredigering klart å kurere musen ved å korrigere genmutasjonen.
Ronald Cohn, førsteforfatter av studien og direktør ved The Hospital for Sick Kids i Toronto, Canada, forteller til den kanadiske nyhetsstasjonen CTV, at han aldri hadde trodd at det ville komme en dag hvor teknologien kom så langt at man kunne rette opp i en genetisk mutasjon.
Genfeil i muskelprotein
Forskningsinnsatsen startet med at Cohns team fikk donert en genetisk prøve fra en 19 år gammel gutt med Duchennes muskeldystrofi.
DMD er en genetisk lidelse som gjør at musklene i kroppen degeneres over tid. Man har fremdeles ikke funnet noen kur mot denne sykdommen.
Mutasjonen sitter på X-kromosomet og rammes derfor nesten bare gutter.
DMD forårsakes av feil i genet til et muskelprotein, kalt dystrofin, men for 10- til 15 prosent av pasientgruppen, inkludert 19-åringen, forårsakes det av en duplikasjonsmutasjon, hvor deler av genet oppstår to ganger.
DMD kan også forårsakes av andre mutasjoner som påvirker dystrofin-genet.
Cohn og hans forskningsgruppe klarte ved hjelp av den donerte prøven å gjenskape den 19 år gamle pasientens duplikasjonsmutasjon hos en laboratoriemus.
Forskerne injiserte deretter et CRISPR-molekyl inn i musen, som var designet på en måte som gjorde at det skulle eliminere mutasjonen, og forhåpentligvis også gjenopprette normal funksjon i genet.
Dramatisk effekt
Før- og etterbilder viser en dramatisk forskjell på musens muskelstyrke og kondisjon. Etter CRISPR-behandlingen forsvant alle tegn til svakhet i musklene hos musen.
Hvis man ser på spekteret av genetiske lidelser, er cirka ti prosent forårsaket av det man kaller duplikasjonsmutasjoner, forteller Kohn. Konseptet og metodologien som ligger bak denne teknologien kan i teorien benyttes på alle slike mutasjoner.
Ronald Cohn sier at neste steg er å utvikle denne teknologien til en medisin, og deretter ha som målsetning å sette igang kliniske studier.































































