Legemidler og biotek
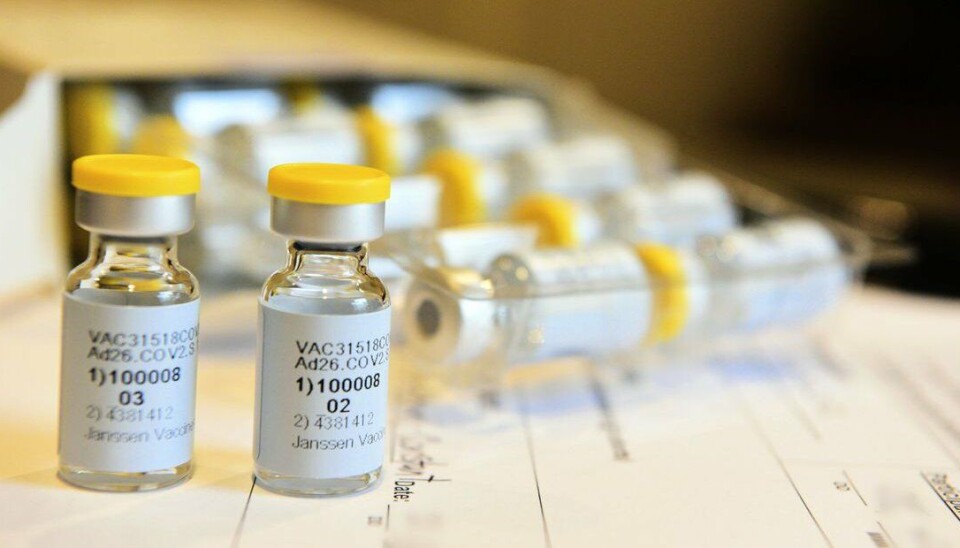
Johnson & Johnson setter coronavaksine-studie på pause etter «uforklarlig sykdomstilfelle»
Johnson & Johnson har satt sin avsluttende vaksinestudie på pause etter at de har oppdaget sykdom hos en av deltagerne.
Det bekrefter Johnson & Johnson i en pressemelding natt til tirsdag.
– Vi har midlertidig stoppet videre tester av alle våre kliniske studier med Covid-19-vaksinen, inkludert vaksinen i fase 3, på grunn av en uforklarlig sykdom hos en av deltagerne. I henhold til våre retningslinjer blir sykdommen undersøkt og evaluert av uavhengige Data Stafety Monitoring Board, skriver selskapet.
Vaksinen er inne i den avsluttende fase III studien før den deretter kan bli godkjent av de amerikanske og europeiske legemiddelmyndighetene. Fase III studien startet 21. september. Pausen betyr at nettpåmeldingen til å delta i studien, som har plass til 60.000 frivillige, er blitt stengt. Pausen vil pågå mens en uavhengig pasientsikkerhetsnemnd har satt seg inn i saken.
Johnson & Johnson har ikke ønsket å gi ytterligere informasjon om den uforklarlige sykdommen på grunn av personvernet.
– Vi må respektere studiedeltagerens privatliv. Vi undersøker også deltagerens sykdom, og det er viktig at vi har alle fakta på bordet før vi kommer med mer informasjon. Bivirkninger, sykdom, ulykker og så videre, selv alvorlige, er forventet i kliniske studier, spesielt de store studiene, skriver selskapet i pressemeldingen
Johnson & Johnson er en av flere legemiddelprodusenter som har inngått avtale med blant annet USAs myndigheter og EUs vaksinesamarbeid som også skal gi Norge tilgang på koronavaksiner når de er ferdigutviklet og godkjent. Den 8. oktober inngikk EU en avtale om kjøp på opptil 400 millioner doser til alle EU-land og Norge, hvis vaksinen er trygg og effektiv mot Covid-19. USA har gjennom Operation Warp Speed bestilt 100 millioner. Dette er også en av vaksinene Storbritannia satser på.
Senest i september satt legemiddelselskapet AstraZenecas sin såkalte Oxford-vaksine på vent etter mistanke om alvorlige bivirkninger hos testpersoner i Storbritannia.
Få dager senere ble testingen startet opp igjen.































































