Coronaviruset
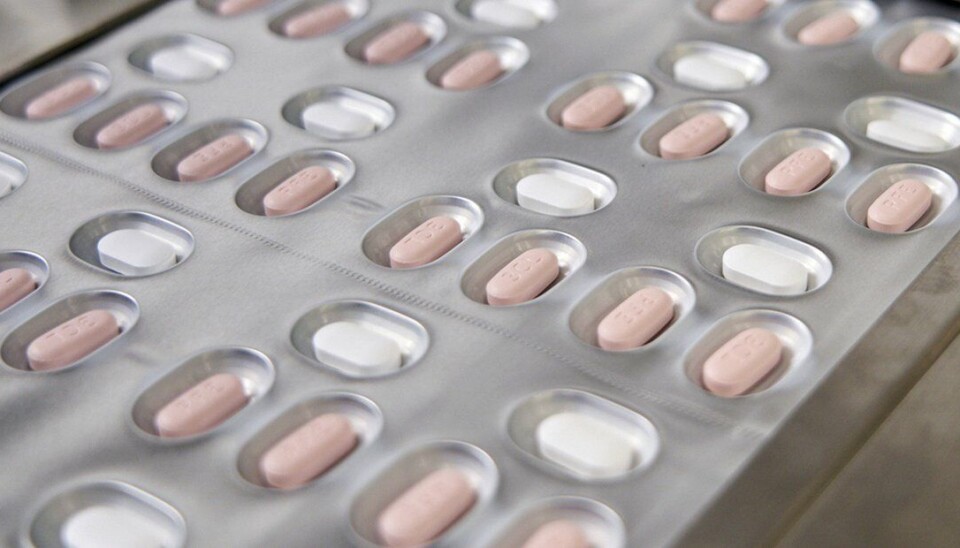
EMA anbefaler Pfizers tablettbehandling mot covid-19
Det europeiske legemiddelverket EMA anbefaler godkjenning av det antivirale legemidlet Paxlovid mot koronavirussykdom.
EMAs vitenskapelige komité for legemidler (CHMP) anbefaler Pfizers antivirale tablettbehandlingen Paxlovid.
Pfizer sier at de forventer at EU-kommisjonen raskt gir sin tilslutning til innføring hvilket vil innebære at Paxlovid bli den første orale behandlingen mot covid-19 som kan tas i bruk i EU- og EØS-landene.
Tillitserklæring
– Denne tillitserklæringen til Paxlovid kommer i et kritisk øyeblikk når Europa fortsetter å ta tak i utfordringene med pandemien og i en tid da spredningen av smitte øker i mange land rundt om i verden, sier Albert Bourla, administrerende direktør i Pfizer.
- Vi er stolte over å ha stor produksjonskapasitet i Europa og forventer å produsere opptil 120 millioner behandlingskurer med Paxlovid globalt. I påvente av en betinget markedsføringstillatelse fra EU-kommisjonen, vil vi fortsette å jobbe tett med myndighetene i EUs medlemsland for å sikre at denne viktige behandlingen kan gjøres tilgjengelig for pasienter over hele Europa så snart som mulig, sier han.
Norge har meldt inn et behov til EU om 41.000 doser av Pfizers koronapille i første og andre kvartal i 2022.
CHMP baserte sin positive anbefaling på de vitenskapelige arbeidene som støtter Paxlovid, inkludert data fra fase 2/3 EPIC-HR-studien (Evaluering av proteasehemming for COVID-19 hos høyrisikopasienter), som inkluderte ikke-innlagte voksne i alderen 18 år og eldre med bekreftet covid-19 som har økt risiko for å utvikle alvorlig sykdom. Data viste at Paxlovid reduserte risikoen for sykehusinnleggelse eller død med 89 prosent (når behandlingen ble igangsatt innen tre dager etter symptomdebut) og 88 prosent (når behandlingen ble igangsatt innen fem dager etter symptomdebut) sammenlignet med placebo, uten noen dødsfall i behandlingsgruppen.
Milde bivirkninger
Behandlingsrelaterte bivirkninger var sammenlignbare mellom Paxlovid (23 %) og placebo (24 %), hvorav de fleste var milde. Studien er sendt til en fagfellevurdert publikasjon. Ytterligere kliniske fase 2/3-studier pågår hos voksne med standardrisiko (dvs. lav risiko for sykehusinnleggelse eller død) som kan utvikle seg til en alvorlig sykdom, og hos de som har blitt eksponert for viruset i husholdningen.
Bourla forteller at Pfizer vil så lenge pandemien pågår tilby sin tablettbaserte behandling gjennom en differensiert prismodell basert på lands inntektsnivåer for å fremme rettferdig tilgang over hele verden. Det betyr at høy- og mellominntektsland vil betale mer enn lavinntektsland.
Pfizer har inngått en avtale med Medicines Patent Pool (MPP), en FN-støttet organisasjon som arbeider for å gjøre medisinsk behandling og teknologi globalt tilgjengelig. Lisensavtalen som Pfizer har inngått med MPP utvider tilgangen til Paxlovid i 95 lav- og mellominntektsland, som utgjør om lag 53 prosent av verdens befolkning.
































































