Legemidler og biotek
USA har godkjent den første CAR-T celleterapien for pasienter med benmargskreft
Det amerikanske legemiddelverket, FDA, har godkjent den første persontilpassede celleterapien for behandling av pasienter med avansert myelomatose. Det er ventet at Abecma snart får markedsføringstillatelse i Europa og dermed også i Norge.
Bristol Myers Squibb og Bluebird Bio som har utviklet behandlingen vil markedsføre den under merkenavnet Abecma.
Det pågår en klinisk studie med Abecma på Oslo Myelomatosesenter, men om behandlingen blir innført i Norge er usikkert.
Beslutningsforum har bare innført én CAR-T behandling
For at norske myelomatosepasienter skal få tilgang til behandlingen er det ikke tilstrekkelig med en norsk markedsføringstillatelse, Abecma må også få et positivt vedtak i Beslutningsforum.
Statens legemiddelverk fikk i oktober i fjor oppdrag å gjennomføre en helseøkonomisk vurdering (hurtig metodevurdering) av Abecma. Selv om behandlingen er effektiv er den også svært kostbar. Abecma som er en engangsinfusjon, er av produsentene oppgitt til å koste 419 500 dollar - 3,6 millioner kroner - og Beslutningsforum har tidligere vendt tommelen ned for å innføre CAR-T celleterapier for andre diagnoser fordi prisen har vært for høy.
Behandling med gen-, celle- eller vevsterapi klassifiseres som Advanced Therapy Medicinal Products (ATMP), eller på norsk avanserte legemidler. Beslutningsforum har så langt bare innført én ATMP, og det er celleterapien/CAR-T behandlingen Kymriah til behandling av akutt lymfoblastisk leukemi (ALL) for barn og unge. Godkjenningen kom i desember 2018, men i september 2019 fikk både Kymriah og Yescarta - en annen CAR-T - nei av Beslutningsforum til behandling av storcellet B-cellelymfom.
Innført som femtelinjebehandling
Myelomatose eller benmargskreft, er den vanligste av blodkreftsykdommene med 450 nye tilfeller hvert år. Den er en kreftsykdom som dannes i plasmacellene, en type hvite blodlegemer som hjelper til med å bekjempe infeksjoner. Hos mennesker med myelomatose akkumuleres ondartede plasmaceller i benmargen, der de fortrenger friske blodceller og forårsaker svulster, nyreskade, ødeleggelse av bein og nedsatt immunforsvar.
Abecma er nå godkjent av FDA for å behandle pasienter med myelomatose som ikke lenger reagerer på fire eller flere tidligere behandlingslinjer.
Genmodifiserer pasientenes immunceller
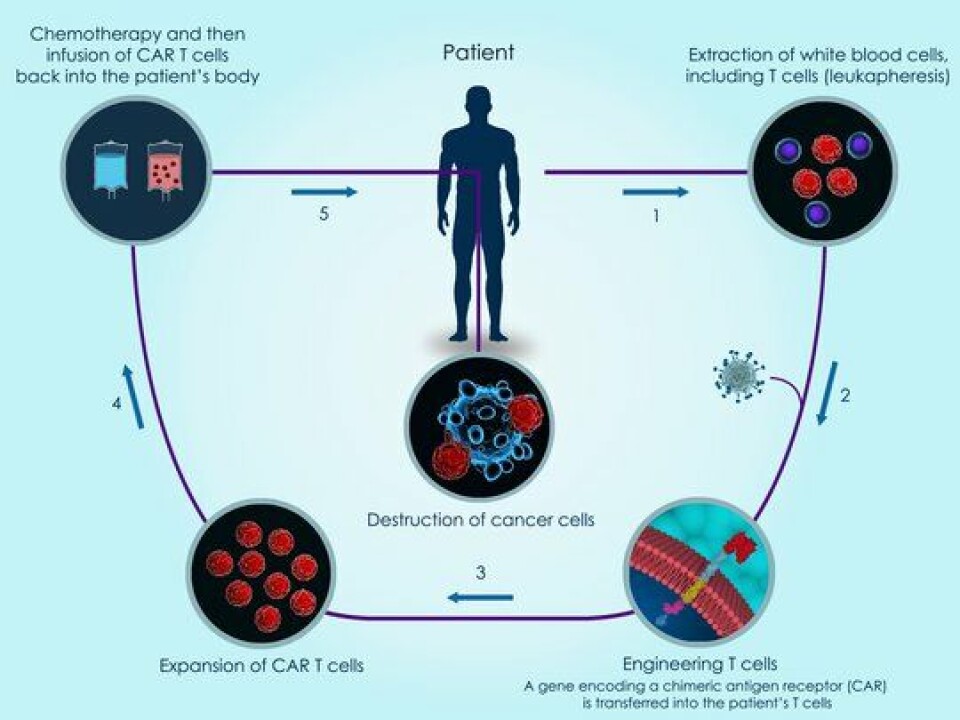
Abecma lages ved først å hente ut ut hvite blodlegemer - immunceller/T-celler - fra pasienter med myelomatose. I et avansert laboratorium endres T-cellene genetisk slik at de gjenkjenner et protein kjent som BCMA (B-celle modning antigen) som finnes på myelomatose-kreftcellene - de ondartede plasmacellene. Det skjer ved at et nytt gen blir satt inn i T-cellene. Til slutt føres millioner av slike immunceller tilbake i kroppen til pasienten og de ombygde immuncellene finner og dreper BCMA-holdige celler.
Den første CAR-T behandlingen som retter seg mot BCMA
Dette er den første godkjente CAR-T som retter seg mot BCMA-proteinet. De fire andre CAR-T-behandlingene som fra før er godkjent i USA (to fra Gilead, én fra Novartis og én fra Bristol Myers Squibb) og de tre som er godkjent i Europa er alle laget på samme måte som Abecma, men T-cellene er konstruert for å målrette mot et protein som heter CD19 som finnes på lymfomkreftceller.
7 av 10 oppnådde respons
FDA sin godkjenning baserer seg på den sentrale fase 2-studien KarMMa som inkluderte 128 pasienter. Pasientene i studien fikk en av tre doseringsnivåer som varierte fra 150 til 450 millioner T-celler. Flertallet av pasientene oppnådde “rask, dyp og vedvarende respons” opplyser Bristol Myers Squibb og Bluebird Bio i en pressemelding. Responsraten var 73%, inkludert en komplett responsrate på 28%. Median responsvarighet var 11 måneder. Pasientene levde median nesten ni måneder uten at sykdommen forverret seg - et mål kalt progresjonsfri overlevelse. Pasientene som i studien ble behandlet med den høyeste dosen hadde en responsrate på 82%, inkludert komplett responsrate på 39%. Disse pasientene levde median ett år uten at sykdommen forverret seg.
En pasient i studien døde av et alvorlig tilfelle av cytokinstorm, en immunreaksjon som ofte er assosiert med CAR-T-behandling. Samlet sett ble moderat til alvorlig cytokinstorm rapportert hos i underkant av 6% av pasientene. Tre prosent av pasientene rapporterte høyverdig nevrotoksisitet, en annen bivirkning som ofte ses i CAR-T terapi.
Studien ble pubisert i New England Journal of Medicine i februar.
- CAR-T-celleterapier har vist et grensesprengende potensiale for behandling av blodkreft. Vi er stolte over å kunne tilby den første CAR-T celleterapien til myelomatosepasienter som har gjennomgått flere behandlingslinjer, som gir muligheten for langvarig effekt, sier Samit Hirawat som er Bristol Myers Squibbs sjefslege.
Pågående studie i Norge
- CAR-T celleterapi er en svært lovende behandling innen myelomatose, sier overlege Fredrik Schjesvold på Oslo myelomatosesenter. Nå har senteret startet en pasientstudie med Abecma. De første pasientene som er valgt startet behandlingen i begynnelsen av november. To tredeler av pasientene skal få CAR-T-behandling med Abecma. En tredjedel får standard behandling. Studien er global og såkalt «open label» som betyr at både behandlere og pasienter vet hvilken medisin som gis.
Får snart konkurranse
Abecma vil sannsynligvis få konkurranse i nær fremtid. Legemiddelselskapet Janssen forventes å sende inn søknad til FDA og EMA på sin egen BCMA-målrettede CAR-T-behandling cilta-cel senere i år.
Den kliniske studien til Janssen heter CARTITUDE-1 og pasienter fikk én infusjon av cilta-cel. 97 prosent av pasientene oppnådde respons av behandlingen, og 67 prosent oppnådde komplett respons (CR) hvilket betyr at de ikke hadde noe tegn til kreftceller i benmargen.
‘Det faktum at Abecma har blitt presset langt ut i behandlingskjeden (femtelinjebehandling) kan gi Janssen en fordel med sin rivaliserende BCMA CAR-T terapi hvis den oppnår en indikasjon tidligere i behandlingskjeden. Når pasienter går over i senere behandlingslinjer, er det mindre sannsynlig at de svarer på behandlingen - og når de gjør det, varer responsraten vanligvis ikke så lenge.
Hans Anderssen, redaktør i HealthTalk

Vi i HealthTalk ønsker å lage innhold som er verdifullt for deg som jobber i helsevesenet. Hvis du likte denne artikkelen, og vil at vi skal lage mer innhold som dette, kan du støtte oss ved å melde deg på vårt nyhetsbrev her
































































