Legemidler og biotek

Beslutningsforum innfører lorlatinib til behandling av avansert ALK lungekreft
Pasienter med avansert ALK-mutert ikke småcellet lungekreft fikk i dag et nytt behandlingstilbud. Beslutningsforum sa i dag ja til Pfizers lorlatinib (Lorviqua) som andrelinjebehandling.
På dagens møte hadde Beslutningsforum hele 10 metoder til vurdering. Det ble ja til åtte, mens to fikk nei. Lorlatinib var et av legemidlene som ble innført.
Dette er andre gang denne behandlingen er oppe til vurdering. 27 januar 2020 sa Beslutningsforum nei til å innføre behandlingen, og begrunnet avslaget med at det ikke forelå tilstrekkelig effektdokumentasjon og at prisen var for høy sammenlignet med dagens standardbehandling.
22 pasienter er aktuelle
Lorlatinib er et målrettet legemiddel som brukes til behandling av voksne med fremskredne stadier av ikke-småcellet lungekreft. Lorlatinib hemmer en type enzym som kalles tyrosinkinase og gjør at kreftcellene dør hos pasienter med endringer i genet for ALK. Lorlatinib gis kun til pasienter der sykdommen skyldes en endring i genet for ALK tyrosinkinase. Behandlingen er ikke kurativ, men livsforlengende, symptomforebyggende og symptomlindrende.
Medikamentet har markedsføringstillatelse for ALK-lungekreft ved progresjon etter alektinib eller ceritinib brukt i førstelinje, og ved progresjon etter crizotinib og minst en annen ALK-hemmer.
Effekten av lorlatinib til andrelinjebehandling av pasienter med ALK-positiv NSCLC er dokumentert gjennom den enarmede studien Profile 1001. Foreløpig resultater fra studien viser objektiv responsrate (ORR) på 42,9 % og progresjonsfri overlevelse (PFS) på 5,5 måneder med lorlatinib.
I følge Statens legemiddelverk er om lag 22 pasienter aktuelle for andrelinjebehandling med lorlatinib hvert år i Norge. Budsjettkonsekvensen vil være på om lag 12 millioner kroner i året.
Pågående førstelinjestudie
Aktuell pasientgruppe er liten og trolig tidsbegrenset på grunn av en pågående studie - CROWN fase 3 studien - der lorlatinib er testet ut i førstelinje ALK-positiv ikke-småcellet lungekreft.
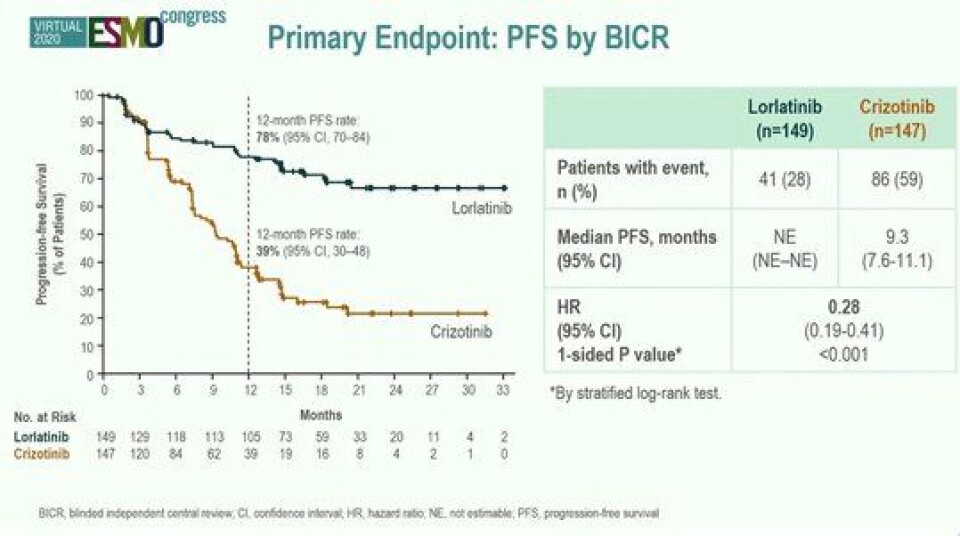
CROWN-studien ble presentert under ESMO i september i år. Den viser at legemidlet øker progresjonsfri overlevelse blant tidligere ubehandlede pasienter. Totalt 296 nydiagnostiserte pasienter med avansert ALK-positiv ikke-småcellet lungekreft ble randomisert 1:1 for å motta enten oral lorlatinib 100 mg én gang daglig eller oral crizotinib (Xalkori) 250 mg to ganger daglig.
Resultatene som ble presentert på ESMO viste at lorlatinib signifikant forbedret progresjonsfri overlevelse (PFS) hos ikke tidligere behandlede pasienter med avansert ALK-positiv ikke-småcellet lungekreft i forhold til crizotinib (placebo). PSF for lorlatinib var etter 12 måneder 78 prosent, mens den var 39 prosent med crizotinib. Median PFS kan ikke estimeres og tallene for totaloverlevelse (OS) var ved analysetidspunktet umodne.
2-5 prosent av pasientene har ALK-mutasjon
Lungekreft er den nest hyppigste kreftformen hos både menn og kvinner i Norge og er den kreftformen som tar flest liv. Den står for 20 prosent av dødsfallene av kreft her i landet. I 2018 ble det registrert 3351 nye tilfeller av lungekreft. Sykdommen forårsaket 2138 dødsfall - 974 kvinner og 1164 menn døde av lungekreft i 2017 – flere enn noen annen kreftform. Ikke-småcellet lungekreft (NSCLC) er den vanligste typen som rammer 80-85 % av lungekreftpasienter.
I følge Norsk kreftregister har om lag 70 % av alle pasienter med NSCLC et langtkommet stadium (stadium IIIb-IV) allerede ved diagnosetidspunktet, og kurativ behandling ikke er mulig. Fem-års overlevelse hos denne pasientgruppen er lav, med ett-års overlevelse etter behandling på under 30 %. For NSCLC er langtidsoverlevelse ved begrenset sykdom 15 % og ved utbredt sykdom er den 0–1 %. I perioden 2007-11 var fem-års relativ overlevelse for alle stadier 12,1 % for menn og 16,8 % for kvinner.
Lungekreft har mange små pasientgrupper som kan ha nytte av målrettet behandling. Om lag 2-5 % av pasientene med ikke-småcellet lungekreft har den spesielle genforandringen kalt ALK-mutasjon som synes å være hyppigere hos yngre ikke-røykende pasienter med avansert sykdom, men kan forekomme i alle aldre og også hos røykere.
Målrettet behandling som krever gentest
Lorlatinib er et målrettet legemiddel som brukes til behandling av voksne med fremskredne stadier av ikke-småcellet lungekreft. Lorlatinib hemmer en type enzym som kalles tyrosinkinase og gjør at kreftcellene dør hos pasienter med endringer i genet for ALK. Lorlatinib gis kun til pasienter der sykdommen skyldes en endring i genet for ALK tyrosinkinase. Behandlingen er ikke kurativ, men livsforlengende, symptomforebyggende og symptomlindrende.
Ifølge nasjonale retningslinjer skal alle pasienter med ikke-småcellet lungekreft som ikke er plateepitelkarsinom testes for EGFR- ROS1- og ALK-mutasjoner.
Dagens behandling av pasienter med verifisert ALK-mutasjon består av TKI-behandling med crizotinib i førstelinje inntil progresjon, etterfulgt av ceritinib eller alectinib. I videre linjer kan platinumdublett være aktuelt etterfulgt av immunterapi hos pasienter med påvist PDL1-uttrykk i tumor. Immunterapi direkte etter ALK-hemmer anbefales ikke grunnet antatt lave responsrater uavhengig av PD-L1 uttryk
Disse fikk ja
Disse legemidlene fikk ja under dagens møte i Beslutningsforum
- Avelumab (Bavencio) til andrelinjebehandling av metastatisk merkelcellekarsinom
- Hyberbar oksygenbehandling av kronisk strålecystitt.
- Lorlatinib (Lorviqua) til ALK-positiv avansert ikke-småcellet lungekreft (NSCLC) i andre – eller senere behandlingslinjer.
- Baricitinib (Olumiant) til behandling av alvorlig atopisk dermatitt hos voksne som er aktuelle for systemisk behandling
- Treosulfan (Trecondi) i kombinasjon med fludarabin til forbehandling (kondisjonering) før allogen hematopoetisk stamcelletransplantasjon (allo HSCT) hos voksne pasienter med malign eller ikke – malign sykdom, og hos pediatriske pasienter eldre enn én måned med malign sykdom.
- Zanamivir (Dectova) til behandling av pasienter i sykehus med alvorlig influensa A eller B-infeksjon.
- Sekukinumab (Cosentyx) til behandling av moderat til alvorlig plakkpsoriasis hos barn og ungdom fra seks år som er aktuelle for systemisk behandling.
- Humant fibrinogen og humant trombin (VeraSeal) for å oppnå lokal stans av blødning (hemostase) under kirurgi.
Disse fikk nei
Disse fikk nei under dagens møte i Beslutningsforum
- Tafamidis (Vyndaqel) til behandling av voksne pasienter med transtyretinamyloidose og kardiomyopati (ATTR-CM).
- Talazoparib (Talzenna) til behandling av voksne pasienter med kimcelle BRCA1/2-mutasjoner som har HER2-negativ lokalavansert eller metastatisk brystkreft.